在相同温度和压强下,对反应CO2(g)+3H2(g) CH3OH(g)+H2O (g)进行甲、乙、丙、
CH3OH(g)+H2O (g)进行甲、乙、丙、
丁四组实验,,实验起始时放入容器内各组分的物质的量见下表
| 物质的量 |
CO2 |
H2 |
CH3OH(g) |
H2O |
| 甲 |
a mol |
a mol |
0 mol |
0 mol |
| 乙 |
2a mol |
a mol |
0 mol |
0 mol |
| 丙 |
0 mol |
0 mol |
a mol |
a mol |
| 丁 |
a mol |
0 mol |
a mol |
a mol |
上述四种情况达到平衡后,n(CH 3OH)最大的是
3OH)最大的是
A.甲 |
B.乙 | C.丙 | D.丁 |
下列离子方程式正确的是( )
| A.硅酸钠溶液中通入过量的CO2 SiO32一 + CO2+2H2O= H2SiO3↓十HCO3一 |
| B.烧碱溶液腐蚀玻璃: SiO2+ 2OH一= SiO32一+ H2O |
| C.碳酸钡与盐酸反应: CO32一+2H+= CO2 ↑+ H2O |
| D.过氧化钠与水反应:2O22—+2H2O ="=" 4OH-+O2↑ |
碳酸氢钠受热容易分解为碳酸钠。现加热5.00 g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31g,则原混合物中碳酸钠的质量为( )
| A.3.38 g | B.4.58 g | C.4.16 g | D.4.41 g |
2003年10月15日,我国成功发射“神舟五号”载人飞船,飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为:2NH4ClO4N2↑+Cl2↑+2O2↑+4H2O。下列有关叙述正确的是()
| A.该反应属于分解反应、氧化还原反应 |
| B.上述反应瞬间能产生大量的热,高温是推动飞船飞行的主要因素 |
| C.铝粉的作用是,点燃时可以置换出氧气 |
| D.在反应中NH4ClO4仅起到氧化剂作用 |
下列反应的离子方程式书写正确的是()
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O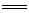 AlO2-+4NH4++2H2O AlO2-+4NH4++2H2O |
B.澄清石灰水与过量苏打溶液混合:Ca2++OH-+HCO3-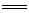 CaCO3↓+H2O CaCO3↓+H2O |
| C.钠投入硫酸铜溶液中:2Na+Cu2+══ Cu+2Na+ |
D.氯化亚铁溶液中通入氯气:2Fe2++Cl2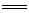 2Fe3++2Cl- 2Fe3++2Cl- |
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是()
①NaHCO3②Al2O3③Al(OH)3 ④NaAlO2 ⑤Al ⑥AlCl3
| A.①③④ | B.①②③④ | C.①②③⑤ | D.全部 |