下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A.H2+CuO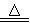 Cu+H2O Cu+H2O |
B.2Na2O2+2H2O===4NaOH+O2↑ |
C.2KClO3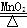 2KCl+3O2↑ 2KCl+3O2↑ |
D.2NaOH+Cl2===NaCl+NaClO+H2O |
HClO是比H2CO3还弱的酸,下列反应Cl2+H2O HCl+HClO达到平衡后,要使HClO的浓度增大,可采取的措施是
HCl+HClO达到平衡后,要使HClO的浓度增大,可采取的措施是
| A.光照 | B.加入NaOH固体 | C.加入水 | D.加入CaCO3固体 |
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量多 |
| B.依据焓判据即可判定(NH4)2CO3受热分解可自发进行 |
| C.热化学方程式未注明温度和压强,△H表示标准状况下的数据 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液,其中pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
| A.HX、HZ、HY | B. HY、HZ、HX |
| C. HX、HY、HZ | D. HZ、HY、HX |
可逆反应∶2NO2 2NO+O2在密闭容器中反应,达到平衡状态的标志是:
2NO+O2在密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ |
| C.①③④ | D.①②③④⑤⑥ |
下列事实不能用电化学理论解释的是
| A.镀层被划破后,镀锌的铁制品比镀锡的铁制品耐腐蚀 |
| B.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| C.铝片不用特殊方法保存 |
| D.锌跟稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快 |