NA代表阿伏加德罗常数,下列说法中,正确的是
| A.2.7g金属铝变成铝离子时失去的电子数目为0.1NA(提示:M(Al)=27g/mol) |
| B.17g氨气所含的电子数目为10NA(提示:M(NH3)=17g/mol) |
| C.2g氢气所含原子数目为NA(提示:M(H2)=2g/mol) |
| D.常温常压下,11.2L氮气所含的原子数目为NA |
0.75 mol·L-1的NaOH溶液200 mL和0.5 mol·L-1的H3PO4溶液200 mL混合,生成盐的物质的量浓度接近()
| A.NaH2PO4和Na2HPO4溶液的浓度均为0.2 mol·L-1 |
| B.Na2HPO4和NaH2PO4溶液的浓度均为0.125 mol·L-1 |
| C.0.15 mol·L-1的Na2HPO4和0.10 mol·L-1的NaH2PO4 |
| D.0.1 mol·L-1的Na2HPO4和0.1 mol·L-1的Na3PO4 |
下列离子方程式不正确的是()
| A.铜与稀硝酸反应 3Cu+8 H++2 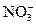 ="===3" Cu2++2NO↑+4H2O ="===3" Cu2++2NO↑+4H2O |
B.稀盐酸与氨水反应H++NH3·H2O====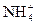 +H2O +H2O |
C.硫酸铵溶液中加入稀氢氧化钠溶液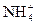 + OH-====NH3↑+H2O + OH-====NH3↑+H2O |
D.磷酸钙与过量的磷酸反应Ca3(PO4)2+4H3PO4====3Ca2++6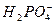 |
下列变化不可能一步实现的()
| A.N2→NH3 | B.N2→NO2 | C.NH3→NO | D.NO2→HNO3 |
实验室存放下列物质常用水封,其中正确的是()
①液溴②浓硝酸③金属钠④白磷⑤红磷⑥电石⑦硫磺
| A.②③⑥ | B.①⑤⑦ | C.①④ | D.只有④ |
下列各组物质互为同素异形体的是()
| A.红磷和白磷 | B.磷酸和偏磷酸 |
| C.NO2和N2O4 | D.35Cl和37Cl |