对于反应2SO2(g)+O2 (g) 2SO3(g)(放热反应),下列判断正确的是
2SO3(g)(放热反应),下列判断正确的是
| A.2体积SO2和足量O2反应,生成2体积SO3 |
| B.其他条件不变,降低温度,正反应速率增大,逆反应速率减小 |
| C.给定条件下该反应进行的限度为SO2消耗速率等于O2生成速率的两倍 |
| D.平衡时,SO2浓度必定等于O2浓度的两倍 |
下列有关热化学方程式的叙述中,正确的是
| A.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则表示该反应中和热的热化学方程式为 NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=+57.4 kJ/mol |
| B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ/mol,则H2的燃烧热为241.8 kJ/mol |
| D.已知2C(s)+2O2(g)===2CO2(g) ΔH1,2C(s)+O2(g)==="2CO(g)" ΔH2;则ΔH1<ΔH2 |
下列溶液一定呈中性的是
| A.pH=7的溶液 |
| B.c(H+)=10-7 mol·L-1的溶液 |
| C.c(H+)/c(OH-)=10-14的溶液 |
| D.氨水和硫酸铵的混合液中c(NH4+)=2c(SO42-) |
对于可逆反应:2A(g)+B(g) 2C(g) ΔH<0,下列各图正确的是
2C(g) ΔH<0,下列各图正确的是
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是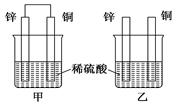
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)===SO2(g)ΔH1=-297.16 kJ·mol-1
②S(正交,s)+O2(g)===SO2(g)ΔH2=-296.83 kJ·mol-1
③S(单斜,s)===S(正交,s) ΔH3
下列说法正确的是
| A.ΔH3=+0.33 kJ·mol-1 |
| B.单斜硫转化为正交硫的反应是吸热反应 |
| C.S(单斜, s)===S(正交,s) ΔH3<0,正交硫比单斜硫稳定 |
| D.S(单斜,s)===S(正交,s) ΔH3>0,单斜硫比正交硫稳定 |