(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。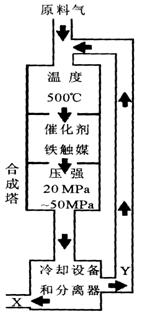
①X的化学式为 ;
②上图中条件选定的主要 原因是(选填字母序号) ;
原因是(选填字母序号) ;
A.温度、压强对化学平衡影响 B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动。下图表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是(选填字母代号) ,当横坐标为温度时,变化趋势正确的是(选填字母序号) 。
(2)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆反应
,
②氨水中水电离出的c(OH-) 10-7mol/L(填写“>”、“<”或“=”);
③将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大以小依次为 。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B两种物质。A为铵盐,B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA。
①写出氨气和氟气反应的化学方程式 ;
②在标准状况下,每生成1 mol B,转移电子的物质的量为 mol。
(9分)芒硝化学式Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为。此时通过阴离子交换膜的离子数(填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钠溶液从出口(填写“A”、“B”、“C”、“D”)导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因。
④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为。已知H2的燃烧热为285.8 kJ/mol,则该燃料电池工作产生36 g H2O时,理论上有kJ的能量转化为电能。
(7分)醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐。
(1)醋酸钠溶液中各离子浓度由大到小的顺序为。
(2)对于醋酸溶液和醋酸钠溶液的下列说法正确的是(填字母,下同)。
| A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小 |
| B.升高温度可以促进醋酸电离,而升高温度会抑制醋酸钠水解 |
| C.醋酸和醋酸钠的混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离 |
| D.醋酸和醋酸钠的混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离 |
(3)物质的量浓度均为 0.1 mol/L 的 CH3COONa 溶液和 CH3COOH 溶液等体积混合(混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是。
(12分)同分异构现象是有机物种类繁多的原因之一,请按要求答题。
(1)C8H10含一个苯环的同分异构体有种,写出其中苯环上的氢被溴取代,所得一溴代物有三种的所有C8H10的名称。
(2)C9H12含一个苯环的同分异构体有种,写出苯环上有3个取代基的所有同分异构体的结构简式。
(3)C10H14含一个苯环的同分异构体有种,写出苯环上只有1个取代基的所有同分异构体的结构简式。
工业上从海水制取溴时,是以氯气氧化海水中的Br-,然后用空气将溴吹出,以碳酸钠溶液吸收。再用硫酸酸化得到单质溴。
(1)写出各步反应的化学方程式。
(2)把滤纸用淀粉和碘化钾的溶液浸泡,晾干后即得淀粉碘化钾试纸。将试纸润湿后,放在盛有溴气的集气瓶口,观察到的现象是,原因是(用化学方程式和必要的文字说明)。
现有0.1mol/L的AlCl3溶液和0.1mol/L的氢氧化钠溶液,进行下面的实验。
(1)在试管中取AlCl3溶液10mL,向其中逐滴加入NaOH溶液,请画出产生白色沉淀物质的量随NaOH溶液加入量变化的趋势图。
(2)向盛有10mLNaOH溶液的试管中滴入AlCl3溶液,边滴加边震荡,产生的现象是_ _;当加入 毫升AlCl3溶液时开始出现沉淀;当加入毫升AlCl3溶液时,产生的沉淀量最多。写出上述过程中所涉及到的的相关离子方程式_ .。