相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g) △H=一92.6kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g) △H=一92.6kJ/mol。实验测得起始、平衡时的有关数据如下表:
| 容器 |
起始各物质的物质的量/mol |
达平衡时体系能量的变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量:23.15kJ |
| ② |
0.9 |
2.7 |
0.2 |
放出热量:Q |
下列叙述不正确的是( )
| A.容器①、②中反应的平衡常数相等 |
| B.平衡时,两个容器中NH3的体积分数均为1/7 |
C.容器②中达平衡时放出的热 量Q=23.15kJ 量Q=23.15kJ |
| D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ |
下列反应的离子方程式正确的是
| A.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O |
| B.在含有Mn2+的溶液中加入酸酸化,再加入PbO2,反应体系显紫红色5PbO2 + 2Mn2+ + 4H+ = 5Pb2+ + 2MnO4— + 2H2O |
| C.碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O |
D.硫化钠水溶液呈碱性的原因:S2-+2H2O  H2S↑+2OH- H2S↑+2OH- |
下列有关物质的性质或应用说法正确的是
| A.氢氧化钠用于治疗胃溃疡病人的胃酸过多症 |
| B.金属钠具有强的还原性,可利用钠和TiCl4溶液反应制取金属Ti |
| C.糖类、油脂、蛋白质在一定条件下均可以水解 |
| D.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
用下列实验装置和方法进行相应实验,能达到实验目的的是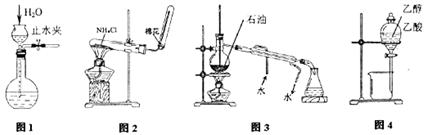
| A.用图1所示方法检查装置的气密性 |
| B.用图2所示装置和方法制取氨气 |
| C.用图3所示装置和方法进行石油分馏 |
| D.用图4装置和方法分离乙醇与乙酸 |
在下列各溶液中,离子一定能大量共存的是:
| A.室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
| B.碱性溶液中:K+、Mg2+、S2-、ClO- |
| C.加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- |
| D.在AlCl3溶液中:K+、Na+、SiO32—、SO42— |
下列说法正确的是
| A.胶体区别于其他分散系的本质特征是分散质微粒直径在1 nm~100 nm之间 |
| B.NH3的沸点高于PH3,是因为N-H键能大于P-H键能 |
| C.金属阳离子只存在于离子晶体中 |
| D.由非金属元素组成的化合物一定是共价化合物 |