(4分)在下列化合物中:H2O、Na2O、I2、、N aCl、、KOH、CO2、NH4Cl、Na2O2,请填空:
aCl、、KOH、CO2、NH4Cl、Na2O2,请填空:
(1)只由非金属组成的离子化合物是 ,
(2)含有极性共价键的离子化合物是 ,
(3)只含有非极性共价键的是 ,
(4)既有离子键又有非极性键的化合物是 。
选用适当的试剂和方法除去下列物质中的杂质(括号内)填下表:
除杂质的试剂:①氢氧化钠溶液②溴水③生石灰④饱和碳酸钠溶液
除杂质的方法:A分液 B萃取 C蒸馏 D过滤
| 混合物 |
除杂质的试剂 |
除杂质的方法 |
| 苯(苯酚) |
(1) |
(4) |
| 酒精(水) |
(2) |
(5) |
| 乙酸乙酯(乙酸) |
(3) |
(6) |
(1)按系统命名法,有机物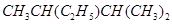 的名称是 。若该有机物是由烯烃加成氢气得来的,那么烯烃的结构有种,若该有机物是由炔烃加成氢气得来的,那么炔烃的结构简式该炔烃与含等物质的量的溴的四氯化碳反应的方程式为
的名称是 。若该有机物是由烯烃加成氢气得来的,那么烯烃的结构有种,若该有机物是由炔烃加成氢气得来的,那么炔烃的结构简式该炔烃与含等物质的量的溴的四氯化碳反应的方程式为
(2)支链只有一个乙基且式量最小的烷烃 的结构简式
氯化钠样品含有少量的Na2SO4和 Na2CO3,按下列流程进行净化,请在流程中的()中写上合适的试剂,在[ ]中写上实验操作名称
写出有关反应的化学方程式:
第步②
第步③
第步⑤
已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器。)
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
| 序号 |
实验步骤 |
简述实验操作(不必叙述如何组装实验装置) |
| ① |
溶解 |
将混合物放入烧杯中,加入98% H2SO4,充分搅拌直到固体不再溶解。 |
| ② |
||
| ③ |
||
| ④ |
||
| ⑤ |
洗涤沉淀 |
|
| ⑥ |
检验沉淀 是否洗净 |
下列提纯方法不正确的是
| A.除去KNO3中的NaCl杂质-----------结晶.重结晶 |
| B.除去食盐中的泥沙-----------过滤 |
| C.除去KCl中的K2CO3------------加适量盐酸 |
| D.除去碘水中的水-----------升华 |