碱石灰是实验室常用的干燥剂。
[提出问题]
实验室中久置的碱石灰样品的成分是什么?
[进行猜想]
久置的碱石灰样品中可能含有CaO、NaOH、
Ca(OH)2、Na2CO3、CaCO3等成分。样品中可能含有Ca(OH)2、Na2CO3的原因是(用化学方程式表示) 、 。
[实验过程] 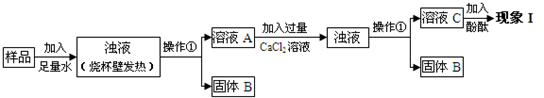
试回答下列问题:
(1)操作①的名称是 。溶液C中加入酚酞的现象I为 。
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有 ,反应的方程式为 。
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是 。
[实验结论] 该久置的碱石灰样品中能确定一定含有的物质是 。(填序号)
| A.CaO | B.NaOH | C.Ca(OH)2 | D.Na2CO3E、CaCO3 |
(5分)阅读下列材料,回答下列问题。
打火机是人们在日常生活中经常使用的一种点火工具。其中一种打火机的主要工作原理是:打火时,按一下打火机,带动齿轮摩擦火石,火石里的金属镧和铈就开始燃烧,迸射出火花,与此同时,保存在打火机里的液体(主要是丁烷)在室温下被汽化释放出来,遇到镧、铈产生的火花燃烧起来,从而完成点火。
(1)可燃物燃烧的两个条件是:;。
(2)根据上述材料判断,金属镧和铈的着火点都(“较高”或“较低”);丁烷的沸点室温(“高于”或“低于”)。
(3)夏天,如果把塑料外壳的打火机放在太阳底下曝晒,常会发生爆炸导致危险,请你分析打火机爆炸的主要原因是。
(8分)某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下充分反应生成CO2来进行分析测定。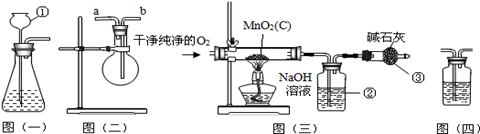
(1)仪器①的名称是。如果该实验选择图(一)装置来制取氧气,该反应的化学方程式为。
(2)用图(二)装置可用于收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从 端通入。
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(生石灰与固体氢氧化钠的混合物),其作用是防止空气中进入②中(填写化学式)。
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为 (填字母)。
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图(三)中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为(填计算结果)。
(5分) 某兴趣小组用右图所示装置发生并收集反应产生的气体,
同时测量其体积。
(1)试写出实验室用该装置,通过置换反应制备初中常见气体的
化学反应方程式。
(2)图示装置对反应物的状态和反应条件的要求是:、。
(3)利用该装置测得反应生成气体体积偏大的最主要原因是:。
(4分)“中国最美丽的乡村”——江西婺源,以“红、绿、黑、白”四大特色而闻名。
(1) “红”指红鲤鱼:食用红鲤鱼可以补充的营养素主要是;
(2) “绿”指婺源绿茶:绿茶中含有儿茶素(C5H14O6·H2O),儿茶素由种元素组成;
(3) “黑”指龙尾砚:罗文金星石头(主要成分是Fe2S)是制作龙尾砚的材料之一,Fe2S中铁元素和硫元素的质量比;
(4)“白”指江湾雪梨,种植雪梨需施适量氮肥。下列化肥中属于氮肥的是:。
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2
(6分)形态各异的物质可按一定规律分类(用序号填空):
A盐酸 B氯化钾 C 氢氧化钙
D甲烷 E.五氧化二磷 F.氮气
| 题号 |
物质分类标准 |
字母序号 |
题号 |
物质分类标准 |
字母序号 |
| (1) |
非金属氧化物 |
(4) |
非金属单质 |
||
| (2) |
易溶性盐 |
(5) |
挥发性酸 |
||
| (3) |
微溶性碱 |
(6) |
最简单的有机物 |