在常温下,纯水中存在电离平衡H2O H++OH-,若要使水溶液的酸性增强,并使水的电离程度增大,应加入的物质是
H++OH-,若要使水溶液的酸性增强,并使水的电离程度增大,应加入的物质是
A.NaHS O4 O4 |
B.KAl(SO4)2 | C.NaHCO3 | D.CH3COONa |
下列有关胶体的说法正确的是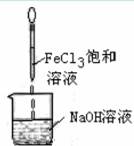
| A.直径介于10-9 m~10-7m之间的微粒称为胶体 |
| B.电泳现象可证明胶体带有电荷 |
| C.用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同 |
| D.Fe(OH)3难溶于水,因此可以用下图的方法制备Fe(OH)3胶体 |
下列关于氧化还原反应说法正确的是
| A.肯定有一种元素被氧化,另外一种或多种元素被还原 |
| B.某元素从化合态变成游离态,该元素一定被还原 |
| C.氧化还原反应的本质是元素的化合价发生改变 |
| D.在反应中不一定所有元素的化合价都发生变化 |
下列事故处理方法正确的是
| A.凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| B.制取并用排水法收集氧气结束后,应立即停止加热 |
| C.浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
| D.浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3 +6HCl=3Cl2+KCl +3H2O,③2KBrO3 +Cl2=Br2+2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.反应②中氧化剂与还原剂的物质的量之比为6∶1 |
| C.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
| D.反应③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
在标准状况下①6.72L CH4②3.01×1023个HCl分子③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是
| A.密度②>③>①>④ | B.体积②>③>①>④ |
| C.质量②>①>③>④ | D.氢原子个数①>③>②>④ |