氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产。氨的水溶液中存在电离平衡,常用电离常数Kb和电离度α来定量表示其电离程度。Kb和α常用的测定方法:在一定温度时用酸度计测定一系列已知浓度氨水的pH,可得各浓度氨水对应的c(OH-),然后通过换算求得各对应的α值和Kb值。下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50 mL碱式滴定管、100mL烧杯、 0.10 mol·L-1氨水
【实验数据】(不必填表格)
| 烧杯号 |
V氨水 (mL) |
V水(mL) |
c (NH3·H2O)(mol·L-1) |
c(OH-) |
Kb |
α |
| 1 |
50.00 |
0.00 |
|
1.34×10-3 |
|
|
| 2 |
25.00 |
25.00 |
|
9.48×10-4 |
|
|
| 3 |
5.00 |
45.00 |
|
4.24×10-4 |
|
|
请根据以上信息回答下述问题:
(1)25℃时,氨水的电离常数:Kb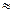 ▲ ,通过计算所得的数据和简洁的文字说明电离常数、电离度与弱电解质的初始浓度的关系 ▲ 。
▲ ,通过计算所得的数据和简洁的文字说明电离常数、电离度与弱电解质的初始浓度的关系 ▲ 。
(2)用0.10mol·L—1盐酸分别滴定20.00mL0.10mol·L—1的NaOH溶液和20.00mL0.10mol·L—1
氨水所得的滴定曲线如下: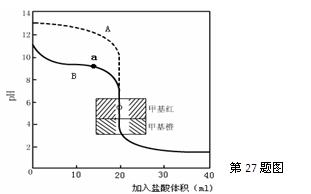
请指出盐酸滴定氨水的曲线为 ▲ (填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序 ▲ 。
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)= 2N2(g)+6H2O(l) △H1 ①
4NH3(g)+5O2(g)= 4NO(g)+6H2O(l) △H2 ②
4NH3(g)+6NO(g)= 5N2(g)+6H2O(l) △H3 ③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= ▲ 。
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料。其总反应式为4NH3+3O2= 2N2+6H2O,正极上的电极反应式为O2+2H2O+4e—=4OH—,则负极上的电极反应式为 ▲ 。
CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0 g CH4完全燃烧生成液体水放出444.8kJ热量。则
CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=kJ·mol-1。
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为,通入b气体的电极反应式为 。(质子交换膜只允许H+通过)
(3)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 。
(4)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96 L CH4可处理22.4 L NOx,则x值为。
T ℃时,向2 L恒容密闭容器中充入1 mol NO2与2mol SO2发生如下反应:
NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=-41.8 kJ·mol-1。
SO3(g)+NO(g) ΔH=-41.8 kJ·mol-1。
(1)下列能说明该反应达到平衡状态的是。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗n mol SO3的同时生成n mol NO2
(2)反应进行到20 s 时,测得反应速率v(NO) =" 0.005" mol·L-1·s-1,则消耗的NO2为mol。
(3)下列措施能使反应加快的是(仅改变一个条件)
a.降低温度b.缩小容积 c.使用效率更高的催化剂
(4)若上述容器为绝热容器(与外界无热交换),则到达平衡所需时间将。
a.延长b.缩短 c.不变 d.无法确定
X、Y、Z、Q、R是原子序数依次增大的短周期主族元素。已知:气体YX3能使润湿的红色石蕊试纸变蓝,Z和X在同一主族,Q原子的最外层电子数是其周期序数的2倍。回答下列问题:
(1)Z原子的结构示意图为,YX3的电子式为(用元素符号表示)。
(2)Z、Q、R原子的半径从大到小的顺序是 (用元素符号表示)。
(3)Q分别与X、Z形成的化合物类型分别为、(填离子化合物或共价化合物)。
(4)能证明R的非金属性比Q强的实验事实是(填字母序号)。
a.HR的水溶液酸性比H2Q的水溶液酸性强
b.R2与H2化合比Q与H2化合容易,且HR的稳定性比H2Q强
c.H2Q的水溶液中通少量的R2气体可置换出单质Q
工业上,可以由下列反应合成三聚氰胺:
CaO+3C CaC2+CO↑;CaC2+N2
CaC2+CO↑;CaC2+N2 CaCN2+C;CaCN2+2H2O=NH2CN+Ca(OH)2
CaCN2+C;CaCN2+2H2O=NH2CN+Ca(OH)2
NH2CN与水反应生成尿素[CO(NH2)2],再由尿素合成三聚氰胺。
(1)写出与Ca在同一周期的Cu原子的基态电子排布式。
(2)写出CaC2中阴离子C22-的一种等电子体的化学式。
(3)1mol 尿素分子[CO(NH2)2]中含有的π键与σ键的数目之比为。
(4)三聚氰胺俗称“蛋白精”,其结构为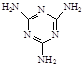 。其中氮原子的杂化方式有。
。其中氮原子的杂化方式有。
(5)CaO晶胞如下图所示,CaO晶体中与O2-距离最近的O2-的个数为。CaO晶体的熔点比NaCl晶体的熔点高的主要原因是。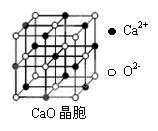
金属单质及其化合物与工农业生产、日常生活有密切的联系。请回答下列问题:
(1)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂,利用如下反应回收燃煤烟气中的硫。反应为:2CO(g)+SO2(g) 2CO2(g)+S(l)△H=-270kJ∙mol-1
2CO2(g)+S(l)△H=-270kJ∙mol-1
其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,不考虑催化剂的价格因素,选择为该反应的催化剂较为合理。(选填序号)
a.Cr2O3b.NiOc.Fe2O3
选择该催化剂的理由是:。
某科研小组用选择的催化剂,在380℃时,研究了n(CO) : n(SO2)分别为1:1、3:1时,SO2转化率的变化情况(图2)。则图2中表示n(CO) : n(SO2)=3:1的变化曲线为。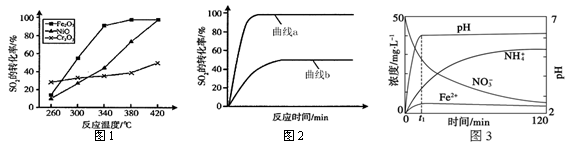
(2)科研小组研究利用铁屑除去地下水中NO3-的反应原理。
①pH=2.5时,用铁粉还原KNO3溶液,相关离子浓度、pH随时间的变化关系如图3(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前发生反应的离子方程式;t1时刻后,反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有明显变化,可能的原因是。
②若在①的反应中加入活性炭,可以提高除去NO3-的效果,其原因可能是。正常地下水中含有CO32-,会影响效果,其原因有:a.生成FeCO3沉淀覆盖在反应物的表面,阻止了反应的进行;b.。
(3)LiFePO4电池具有稳定性高、安全、环保等优点,可用于电动汽车。电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。放电时电池正极反应为。
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。放电时电池正极反应为。