食用油和石蜡油都称为“油”,但从化学组成和分子结构看,它们是完全不同的。下列说法正确的是
| A.食用油属于纯净物,石蜡油属于混合物 | B.食用油属于酯类,石蜡油属于烃类 |
| C.食用油属于有机物,石蜡油属于无机物 | |
| D.食用油属于高分子化合物,石蜡油属于小分子化合物 |
下列电离方程式书写正确的是()
A.HClO  H+ + ClO H+ + ClO  |
B.H2SO  2H+ + SO 2H+ + SO |
C.Ba(OH)2 ="===" Ba +2O +2O +2H +2H |
D.NaHCO ====Na ====Na +H +H +CO +CO |
下列叙述正确的是()
| A.某电解质溶于水后,其导电能力不强,则此电解质必定是弱电解质 |
B.SO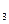 溶于水后,所得溶液导电性很好,故SO 溶于水后,所得溶液导电性很好,故SO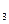 是强电解质 是强电解质 |
| C.共价化合物都是弱电解质 |
| D.弱电解质溶液中,同时存在着电解质电离出来的离子及未电离的分子 |
已知断裂1 mol H—H 键、H—N键分别吸收436 kJ、391kJ热量,根据热化学方程式:N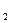 (g)+3H
(g)+3H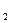 (g)="==" 2NH
(g)="==" 2NH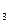 (g)△H= -92.4kJ/mol,则断裂 1 mol N≡N键需要吸收的热量为()
(g)△H= -92.4kJ/mol,则断裂 1 mol N≡N键需要吸收的热量为()
| A.431 kJ | B.649kJ | C.945.6kJ | D.869 kJ |
如果盐酸的浓度是醋酸浓度的二倍,则该盐酸中H
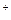 浓度与该醋酸中H
浓度与该醋酸中H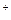 浓度的关系是 ()
浓度的关系是 ()
| A.前者是后者的2倍 | B.前者比后者的2倍大 |
| C.前者比后者的2倍小 | D.无法判断 |
将2.0 mol SO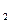 气体和2.0 mol SO
气体和2.0 mol SO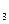 气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)
气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) 2
2 SO3(g),达到平衡时SO3为n mol 。在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是()
SO3(g),达到平衡时SO3为n mol 。在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是()
| A.1.6 mol SO2+0.3 mol O2+0.4 mol SO3 | B.3.0 mol SO2+1.0 mol O2+1.0 mol SO3 |
| C.2.0 mol SO2+1.0 mol O2+2.0 mol SO3 | D.4.0 mol SO2+1.0 mol O2 |