把少量的溴水注入KI溶液中,经充分反应后,加入CCl4振荡,静置后可观察到
| A.液体分成两层,下层呈紫色 | B.液体分成两层,上层呈紫色 |
| C.混合液不分层,且无色透明 | D.混合液不分层,且呈褐色 |
下列中学常见实验的现象或表述正确的是( )
| A.赤铁矿的主要成分是Fe3O4 |
| B.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 |
| C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可 |
| D.除去FeCl3溶液中的FeCl2杂质可以向溶液中加入足量的铁粉,然后过滤 |
下列分子或离子在指定的分散系中一定能大量共存的一组是( )
| A.常温下水电离出的c(H+)·c(OH-)=1×10-20的溶液:Na+、Cl-、S2-、SO32- |
| B.空气:C2H2、CO2、SO2、NO |
| C.含Al3+的无色溶液:Na+、SO42-、K+、ClO-、HCO3- |
| D.高锰酸钾溶液:H+、Na+、SO42-、NO3- |
用NA表示阿伏加德罗常数。下列说法正确的是( )
| A.在含有NA个CH3COO-的醋酸溶液中,H+数目略大于NA |
| B.常温下,5.6 L NO和5.6 L O2的混合气体中含有的分子数为0.5NA |
| C.16.9g BaO2固体中阴、阳离子总数为0.3NA |
| D.含有1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
1mol过氧化钠与2mol碳酸氢钾固体混合后,在密闭容器中加热至250℃充分反应,排出气体物质后冷却,残留的固体物质和排出的气体分别是( )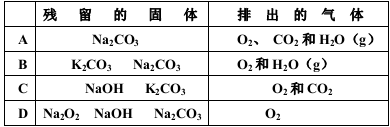
可用于焙烧的装置有以下几种,其中能用于SiO2和NaOH反应的装置为()