小苏打(NaHCO3)是食品工业中一种应用最广泛的疏松剂。资料显示,固态小苏打50℃以上或在潮湿的空气中开始逐渐分解生成碳酸钠、二氧化碳和水,270℃时完全分解。
(1)小苏打、纯碱、烧碱都是化工生产常用试剂,水溶液均显碱性,从物质分类角度看不属于盐的是 ▲ (填写化学式),小苏打的保存应注意 ▲ 。
(2)小苏打(NaHCO3)和纯碱中含钠元素质量分数较大的是 ▲ (填写化学式)。
(3)某化学兴趣小组同学为了对在干燥空气中久置的小苏打样品进行分析,称取一份31.4 g混合均匀的样品,用酒精灯对其充分加热,收集到干燥的CO2气体3.3 g。通过计算判断该小苏打样品是否变质,如果变质计算该样品中NaHCO3质量分数是多少?
某化工厂生产的纯碱中含有少量
杂质,其产品包装袋上标有:碳酸钠≥96%.为了证实该产品中碳酸钠的含量,某同学取12g该样品放入烧杯中,称得烧杯和样品总质量为132.0g再把100g稀盐酸平均分成4次加入烧杯中,每次充分反应后烧杯和剩余物总质量如下:(每次反应产生的
气体都全部从烧杯中逸出)
| 加入稀盐酸次数 |
1 |
2 |
3 |
4 |
| 加入稀盐酸质量/g |
25 |
25 |
25 |
25 |
| 充分反应后烧杯和剩余物总质量/g |
155.2 |
178.4 |
202.6 |
227.6 |
请你根据表中数据分析:①第1次充分反应后产生的
气体质量是g
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)
(1)三氧化硫(
)中,硫元素与氧元素的质量比是,硫元素的质量分数是.
(2)我市某氯碱工厂排放的尾气里含有毒的氯气(
),为防止其污染空气,工厂用20%的
溶液吸收氯气(反应的化学方程式为
).计算:
溶质质量分数为20%的
溶液,理论上可吸收氯气的质量为多少?
某工厂需要280g生石灰( )作干燥剂,需要碳酸钙的质量是多少?至少需要含碳酸钙80%的石灰石(杂质不参加反应)的质量是多少?( )
某纯碱样品中含有杂质
,为测定该样品中
的质量分数,称取纯碱样品
,放入
水中使其完全溶解,再加入稀盐酸
,恰好完全反应,反应后溶液的总质量为
。
试计算:(写出计算过程,结果保留一位小数)
(1)生成二氧化碳的质量;
(2)样品中
的质量分数;
(3)反应后所得溶液中溶质的质量分数。
小宁需要配制80g质量分数为10%的氢氧化钠溶液来制作"叶脉书签".如图是配制该氢氧化钠溶液的实验操作示意图.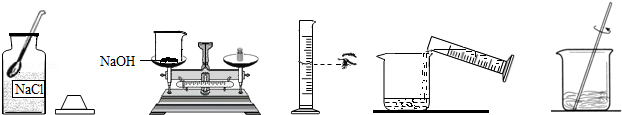
【实验步骤】
(1)计算:需要氢氧化钠固体g,水mL(水的密度以1.0g/cm3计)
(2)称量:用托盘天平称取氢氧化钠固体,用规格为(填"10mL"、"50mL"或"100mL")的量筒取所需要的水,倒入盛有氢氧化钠的烧杯中.
(3)溶解:用玻璃棒搅拌,使氢氧化钠固体完全溶解.
【拓展思维】
假如小宁想用上述配制的氢氧化钠溶液完全中和溶质质量分数为10%的盐酸,至少消耗盐酸的质量是多少?(反应的化学方程式为:
)