某同学在设计实验中使用了以下数据:①用托盘天平称取无水Na2CO3 5.2g ②用量筒取浓盐酸6.34毫升 ③用广泛PH试纸测得的PH值为7.8 ④用盐酸滴定Na2CO3溶液用去盐酸11.20毫升,其中数据不合理的是:
| A.①③ | B.①④ | C.②③ | D.②④ |
铜与1mol/L的硝酸反应,如果NO3-浓度下降0.2mol/L,则溶液中c(H+)同时下降(溶液体积变化忽略不计)()
A.0.2mol·L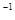 |
B.0.4mol·L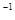 |
C.0.6mol·L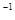 |
D.0.8mol·L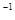 |
用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),则M的相对原子质量为()
A. |
B.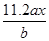 |
C.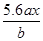 |
D. |
在下列变化①大气固氮②硝酸银分解③实验室制取氨气中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是()
| A.①②③ | B.②①③ | C.③②① | D.③①② |
温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)=PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t / s |
0 |
50 |
150 |
250 |
350 |
| n(PCl3) mol |
0 |
0. 16 |
0. 19 |
0. 20 |
0. 20 |
下列说法正确的是
A.反应在前50 s 的平均速率v(PCl3)=" 0." 0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=" 0." 11 mol·L-1,则反应的△H < 0
C.相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3和0. 20 mol Cl2,反应达到平衡前v(正) > v(逆)
D.相同温度下,起始时向容器中充入2. 0 mol PCl3和2. 0 mol Cl2,达到平衡时,PCl3的转化率小于80%
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下: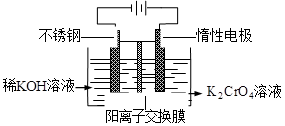
下列说法不正确的是
| A.在阴极式,发生的电极反应为:2H2O+2e-=2OH-+H2↑ |
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2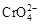 +2H+ +2H+  +H2O向右移动 +H2O向右移动 |
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑ 2K2Cr2O7+4KOH+2H2↑+O2↑ |
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为1-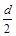 |