常温下,若使pH=3的盐酸与pH=9的Ba(OH)2溶液混合使其成为pH=7的溶液,混合时两溶液的体积比为
| A.1∶60 | B.3∶1 | C.100∶1 | D.1∶100 |
将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08 mol,放出标准状况下气体0.224 L.则下列判断中正确的是
| A.向溶液中滴入KSCN溶液,显红色 |
| B.原混合物中n (Fe)∶n (Fe2O3)=2∶1 |
| C.无法计算原混合物的质量a |
| D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1 |
NH3是一种重要的化工原料,可以制备一系列物质(见图)。下列说法正确的是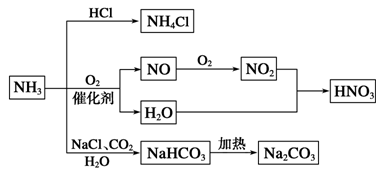
| A.NH4Cl和NaHCO3都是常用的化肥 |
| B.NH4Cl、HNO3和Na2CO3受热时都易分解 |
| C.NH3和NO2在一定条件下可发生氧化还原反应 |
| D.图中所涉及的反应均为氧化还原反应 |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
反应①和②分别是从海藻灰和某种矿石中提取碘的主要反应
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2。
下列说法正确的是
| A.两个反应中均为硫元素被氧化 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
| C.氧化性:MnO2>SO42->IO3->I2 |
| D.反应①、②中生成等量的I2时转移电子数比为1︰5 |
下列选项中,有关实验操作、现象和结论都正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
将过量的CO2通入CaCl2溶液中 |
无白色沉淀出现 |
生成的Ca(HCO3)2可溶于水 |
| B |
常温下将Al片插入浓硫酸中 |
无明显现象 |
Al片和浓硫酸不反应 |
| C |
用玻璃棒蘸取浓氨水点到红色石蕊试纸上 |
试纸变蓝色 |
浓氨水呈碱性 |
| D |
将SO2通入溴水中 |
溶液褪色 |
SO2具有漂白性 |