北京时间3月11日13点46分,日本发生9.0级地震并引发海啸及核泄漏,引起全世界关注。据报道,元素13755Cs是核弹、核武器试验和核反应堆内核裂变的副产品之一,它会释放伽玛射线,13755Cs的半衰期达30年。请问该元素原子内的中子数与电子数之差为
| A.55 | B.27 | C.82 | D.137 |
根据热化学方程式:S(s)+O2(g) SO2(g) ΔH="a" kJ·mol-1(a=-297.2)。分析下列说法,其中不正确的是( )
SO2(g) ΔH="a" kJ·mol-1(a=-297.2)。分析下列说法,其中不正确的是( )
| A.S(s)在O2(g)中燃烧的反应是放热反应 |
B.S(g)+O2(g) SO2(g) ΔH="b" kJ·mol-1,则a>b SO2(g) ΔH="b" kJ·mol-1,则a>b |
| C.1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
| D.16 g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量 |
白磷与氧气可发生如下反应:P4+5O2 P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P
P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P O c kJ·mol-1、O
O c kJ·mol-1、O O d kJ·mol-1。
O d kJ·mol-1。
根据下图所示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )
| A.(6a+5d-4c-12b) kJ·mol-1 |
| B.(4c+12b-6a-5d) kJ·mol-1 |
| C.(4c+12b-4a-5d) kJ·mol-1 |
| D.(4a+5d-4c-12b) kJ·mol-1 |
化学反应N2+3H2 2NH3的能量变化如图所示,该反应的热化学方程式是( )
2NH3的能量变化如图所示,该反应的热化学方程式是( )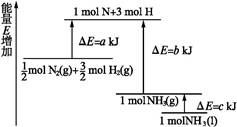
A.N2(g)+3H2(g) 2NH3(l) ΔH=2(a-b-c)kJ·mol-1 2NH3(l) ΔH=2(a-b-c)kJ·mol-1 |
B.N2(g)+3H2(g) 2NH3(g) ΔH=2(b-a)kJ·mol-1 2NH3(g) ΔH=2(b-a)kJ·mol-1 |
C.N2(g)+H2(g) NH3(l) ΔH=(b+c-a)kJ·mol-1 NH3(l) ΔH=(b+c-a)kJ·mol-1 |
D.N2(g)+H2(g) NH3(g) ΔH=(a+b)kJ·mol-1 NH3(g) ΔH=(a+b)kJ·mol-1 |
反应A+B→C(ΔH<0)分两步进行:①A+B→X(ΔH>0),②X→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )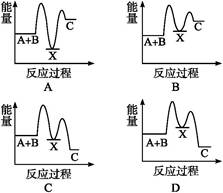
从如图所示的某气体反应的能量变化分析,以下判断错误的是( )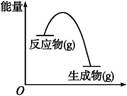
| A.这是一个放热反应 |
| B.该反应可能需要加热 |
| C.生成物的总能量低于反应物的总能量 |
| D.反应物比生成物更稳定 |