某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断
| A.R一定是第四周期元素 |
| B.R一定是ⅣA族元素 |
| C.R的气态氢化物比同族其他元素气态氢化物稳定 |
| D.R气态氢化物化学式为H2R |
下列变化中,一定不存在化学能与热能相互转化的是()。
| A.酸碱中和反应 | B.白磷自燃 | C.燃放爆竹 | D.干冰气化 |
有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
| A.①②③⑤ | B.④⑥⑦⑧ | C.①④⑥⑦ | D.②③⑤⑧ |
将一定量有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤得到沉淀20克,滤液质量比原来石灰水减少5.8克,该有机物可能是()
①乙烯②乙二醇③乙醇④甲酸甲酯
| A.①② | B.①④ | C.②③ | D.②④ |
小红在帮实验员整理化学试剂时,发现一瓶标签破损的无色溶液,标签严重破损,只能隐约看到一部分(如图)。下列说法不正确的是()
| A.该有机物肯定是甲酸乙酯,能发生银镜反应 |
| B.该有机物的分子式为C3H6O2 |
| C.在酸性条件下水解生成两种有机产物的相对分子质量可能相等 |
| D.在碱性条件下可完全水解 |
有关下列两个装置图的说法不正确的是()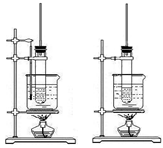
| A.左图可用于实验室制取硝基苯 |
| B.右图可用于实验室制取酚醛树脂 |
| C.长导管是起导气、冷凝回流作用 |
| D.制硝基苯和酚醛树脂均选择浓硫酸作催化剂 |