在一个不传热的固定容积的密闭容器中,可逆反应: N2+3H2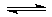 2NH3 ,达到平衡的标志是
2NH3 ,达到平衡的标志是
①反应速率v(N2):v(H2):v(NH3) =" 1" : 3 : 2 ②各组分的物质的 量浓度不再改变
量浓度不再改变
③体系的压强不再发生变化 ④混合气体的密度不变
⑤体系的温度不再发生变化 ⑥ 2V(N2)正= V(NH3)
⑦单位时间内3 mol H—H断键反应同时2 mol N—H也断键反应
| A.①、②、③、⑤、⑥ | B.②、③、⑤、⑥ |
| C.②、③、⑤、⑥、⑦ | D.②、③、④、⑥、⑦ |
当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀又逐渐溶解成为深蓝色的溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀:将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色,根据上述实验现象分析推测,下列描述正确的是( )
| A.Cu2+和Ag+相似,能与NH3结合生成铜氨络离子 |
| B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应 |
| C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下,Cu+只被氧化 |
| D.反应过程中消耗的SO2与生成的SO2的物质的量相等 |
下列分离物质的方法中,根据微粒大小进行分离的是:( )
①分液②过滤③分馏④重结晶⑤渗析
| A.①③⑤ | B.②④ | C.①② | D.②⑤ |
下列推断正确的是( )
| A.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| B.Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 |
| C.CO、NO、 NO2都是大气污染气体,在空气中都能稳定存在 |
| D.SiO2是酸性氧化物,能与NaOH溶液反应 |
已知还原性Cl-<Fe2+<H2O2<I-<SO2,判断下列反应不能发生的是( )
| A.2Fe3++SO2+2H2O=SO42-+4H++2Fe2+ | B.I2+SO2+2H2O=H2SO4+2HI |
| C.H2O2+2H++SO42-=SO2+O2+2H2O | D.2Fe3++2I-=2Fe2++I2 |
下表所列各组物质中,物质之间通过一步反应就能实现如右图所示转化的是( )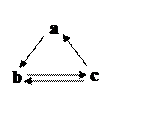
| a |
b |
c |
||
|