一定条件下的反应:PCl5(g)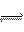 PCl3(g)+C12(g)(正反应吸热)达到平衡后,下列情况使PCl5分解率降低的是:
PCl3(g)+C12(g)(正反应吸热)达到平衡后,下列情况使PCl5分解率降低的是:
| A.温度、体积不变,充入氩气 | B.体积不变,对体系加热 |
| C.温度、体积不变,充入氯气 | D.温度不变,增大容器体积 |
月球土壤中含有较丰富的3 2He,在地球上氦元素主要以42He的形式存在,下列说法正确的是
| A.32He代表原子核内有2个质子和3个中子的氦原子 |
| B.32He和42He互为同位素 |
| C.32He 和42He分别含有1和2个质子 |
| D.32He 的最外层电子数为1,所以32He具有较强的金属性 |
乌头酸的结构简式如图所示,下列关于乌头酸的说法错误的是
| A.化学式为C6H6O6 |
| B.乌头酸能发生水解反应和加成反应 |
| C.乌头酸能使酸性高锰酸钾溶液褪色 |
| D.含l mol乌头酸的溶液最多可消耗3 mol NaOH |
下列有关化学用语的表达中正确的是
A.四氯化碳的电子式: |
B.CH4分子的比例模型 |
C. |
| D.稀硝酸银溶液中滴加过量稀氨水,发生反应的离子方程式为:Ag++2NH3•H2O=[Ag(NH3)2]++2H2O |
一定量的饱和一元醇与足量的钠反应,可得到22.4 L H2(标准状况下)。等量的该醇完全燃烧生成264g CO2,该醇是
| A.1—丙醇 | B.乙醇 | C.1-丁醇 | D.1-戊醇 |
甲酸与乙醇发生酯化反应后生成的酯,其结构简式为
| A.CH3COOCH2CH3 | B.HCOOCH2CH3 | C.CH3COOCH3 | D.HCOOCH3 |