煤的气化是煤高效、洁净利用的方向之一。如图为加热某地煤样所得煤气组成及体积分数随温度变化的曲线图,由图可知该煤气中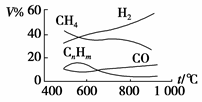
| A.只含有碳、氢两种元素 | B.所含的有机物是CH4、CnHm、CO |
| C.CO体积分数小于CH4体积分数 | D.氢气体积分数最大 |
碳化硅的晶体有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。它与晶体硅和金刚石相比较,正确的是
| A.熔点从高到低的顺序是:金刚石>碳化硅>晶体硅 |
| B.熔点从高到低的顺序是:金刚石>晶体硅>碳化硅 |
| C.三种晶体中的结构单元都是三角锥结构 |
| D.三种晶体都是原子晶体且均为电的良导体 |
下列分子或离子中不能跟质子(H+)结合的是
| A.NH3 | B.H2O | C.HF | D.CH4 |
氯化硼(BCl3)的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120o,它能水解,有关叙述正确的是
| A.氯化硼液态时能导电而固态时不导电 |
| B.氯化硼加到水中使溶液的pH升高 |
| C.氯化硼分子呈正三角形,属非极性分子 |
| D.氯化硼B-Cl之间是sp3形成的σ键 |
下列各组分子中,都属于含极性键的非极性分子的是
| A.CO2、H2S | B.C60、C2H4 | C.C2H4、CH4 | D.NH3、HCl |
下列各组酸中,酸性依次增强的是
| A.H2CO3、H2SiO3、H3PO4 | B.HNO3、H3PO4 、H2SO4 |
| C.HI、HCl、H2S | D.HClO 、HClO3、HClO4 |