用铁片稀H2SO4反应制取氢气时,下列措施不能使氢气生成速率加大的是
| A.加热 | B.不用H2SO4改用98%的浓H2SO4 |
| C.滴加少量CuSO4溶液 | D.不用铁片,改用铁粉 |
下列事实与胶体性质无关的是
| A.在豆浆里加入盐卤做豆腐 |
| B.在河流入海处易形成沙洲 |
| C.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
| D.用一支钢笔使用不同品牌墨水时,容易发生堵塞 |
某溶液中只含下表离子中的几种(不考虑水的电离与离子水解),且各离子的物质的量浓度均为0.1mol/L。
| 阳离子 |
K+ NH4+ Fe2+ Mg2+ Al3+ Cu2+ |
| 阴离子 |
OH- Cl- Al02- CO32- SiO32- SO42- |
某同学进行了如下实验(必要时可加热)
下列说法正确的是
A.原溶液中只含有NH4+ Fe2+ Cl- SO42-
B.由沉淀A推断原溶液中一定含有SO42-
C.滤液A中可能含有K+ Al3+ Cl-
D.沉淀B中一定含有Mg(OH)2
已知部分弱酸的电离平衡常数如下表:
| 弱酸 |
醋酸 |
次氯酸 |
碳酸 |
亚硫酸 |
| 电离平衡常数(25℃) |
Ka=1.75ⅹ10-5 |
Ka=2.98ⅹ10-8 |
Ka1=4.3ⅹ10-7 Ka2=5.61ⅹ10-11 |
Ka1=1.54ⅹ10-2 Ka2=1.02ⅹ10-7 |
下列离子方程式正确的是
A.少量的CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO32-+2HclO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-=SO32-+2HCO3-
D.相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++ HCO3-=CO2↑+2H2O
下列指定反应的离子方程式正确的是
| A.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| C.澄清石灰水中滴加少量NaHCO3: Ca2++ 2OH++2HCO3-= CaCO3↓+2H2O+ CO32- |
| D.向Mg(HCO3)2溶液中加入过量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
下列有关实验装置进行的相应实验,能达到实验目的的是

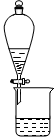
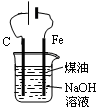
图1图2图3图4
| A.用图1装置制取并收集干燥纯净的NH3 |
| B.用图2所示装置可除去NO2中的NO |
| C.用图3所示装置可分离CH3COOC2H5和饱和碳酸钠溶液 |
| D.用图4装置制备Fe(OH)2并能较长时间观察其颜色 |