下列表示正确的是
A.电解饱和氯化镁溶液的离子方程式是2Cl-+2H2O  H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
B.工业制硫酸过程中,沸腾炉里的反应方程式是2S+3O2  2SO3 2SO3 |
| C.泡沫灭火器的化学反应原理可表示为Al3++3HCO3-=Al(OH)3↓+3 CO2↑ |
| D.表示硫酸与氢氧化钠溶液反应的中和热的热化学反应方程式是 |
H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H="-57.3" kJ/mol
下列说法正确的是
| A.蛋白质、纤维、蔗糖、聚乙烯、淀粉都是高分子化合物 |
| B.研制乙醇汽油(汽油中添加一定比例的乙醇)技术,可以降低机动车辆尾气中有害气体排放 |
| C.使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| D.石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
(1)某温度(t℃)时,测得0.01 mol·L-1的NaOH溶液的pH=13,请回答下列问题:
①该温度下水的Kw=。
②此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va︰Vb=。
(2)已知25°C时Ksp(Mg(OH)2)=1.8×10-11,为除去某食盐溶液中的Mg2+,可用NaOH为除杂试剂,当控制溶液PH=12时,可确保Mg2+除尽,此时溶液中Mg2+的物质的量浓度为.
二氧化锰是制造锌锰干电池的基本原料,普通锌锰干电池的电池反应式为:
2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2。工业上以软锰矿为原料,利用硫酸亚铁制备高纯度二氧化锰的流程如下(软锰矿中所有金属元素在酸性条件下均以阳离子形式存在):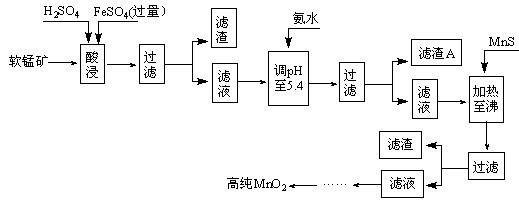
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.24%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物形式完全沉淀时,溶液的pH及部分硫化物的Ksp(均为25℃时)见下表,回答下列问题:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
| pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
8.0 |
| 沉淀物 |
CuS |
ZnS |
MnS |
FeS |
||
| Ksp |
8.5×10-45 |
1.2×10-23 |
1.4×10-15 |
3.7×10-14 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要化学方程式为:
。
(2)滤渣A的主要成分为。
(3)加入MnS的目的是除去杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应式为。
(5)从废旧碱性锌锰电池中可回收利用的物质有(写两种)。
如右图所示,常温,U形管内盛有100mL的某种溶液,
请按要求回答下列问题。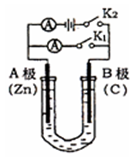
(1)若所盛溶液为CuSO4溶液,打开K2,合并K1,则:
① A为极,B极的电极反应式为。
②反应过程中,溶液中SO42-和OH-离子向极(填:A或B)
移动。
(2)若所盛溶液为滴有酚酞的NaCl溶液,打开K1,合并K2,则:
①A电极可观察到的现象是。
②电解过程总反应的化学方程式是。
③反应一段时间后打开K2 ,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(折算成标准状况)为11.2mL,将溶液充分混合,溶液的pH为。
④向电解后的电解质溶液中加入或通入(填试剂名称),能使溶液复原。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: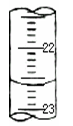
①用0.1000mol/L的标准盐酸润洗酸式滴定管2~3次
②取标准盐酸注入酸式滴定管至“0”刻度以上2~3mL处
③把盛有标准盐酸的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液
④调节液面至“0”或“0”刻度以下,记下读数
⑤取20.00mL待测NaOH溶液注入洁净的锥形瓶中,并加入2~3滴甲基橙试液
⑥把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点,记录滴定管读数
请回答下列问题:
(1)判断到达滴定终点的现象是。
(2)某次滴定时的滴定管中的液面如右图所示,其读数为mL。
(3)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.50 |
25.40 |
| 第二次 |
20.00 |
4.00 |
29.10 |
请计算待测烧碱溶液的浓度为mol/L。
(4)下列实验操作会使实验结果偏高的是。
A、锥形瓶用待测液润洗后再注入待测液
B、酸式滴定管未用标准液润洗,便装入标准液
C、酸式滴定管滴定前俯视读数,滴定后仰视读数
D、酸式滴定管滴定前有气泡,滴定后无气泡