氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:
H2(g)+1/2O2(g)=H2O(l); △H=-285.8 kJ / mol
CO(g)+1/2O2(g)=CO2(g); △H=-283.0 kJ / mol
C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(l);△H=-5518 kJ / mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l); △H=-890.3 kJ / mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是
| A.H2(g) | B.CO(g) | C.C8H18(l) | D.CH4(g) |
下列说法不正确的是
| A.K+与Ar的结构示意图相同 |
B.二氧化碳的电子式: |
C.氧化钠的电子式: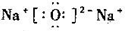 |
D.氯化氢的形成过程: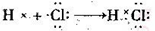 |
下列各反应的能量变化分别用如下形式的示意图表示,其中正确的是
下列备装置中电流表有电流通过的是
下列有关说法正确的是
| A.水分子间的作用力强于分子内的H-O键 |
| B.形成化学键的微粒只能是离子 |
| C.含有离子键的化合物一定是离子化合物 |
| D.共价化合物分子里的化学键只能是极性键 |
已知2 mol H2(g)燃烧生成液态水放出的热量为571.6 lkJ,而2 molH2 (g)完全燃烧生成气态水放的热量为483. 6 kJ。下列说法正确的是
| A.l molH2O (I)变成lmolH2O (g),向外界释放能量 |
| B.1 molH2O (g)分解成H2(g)和O2(g),吸收241. 8 kJ能量 |
| C.2 mol H2(g)和l mol O2(g)的总能量小于2 molH2O(1)的能量 |
| D.断裂2 molH2O (g)中所有的O-H键,吸收483. 6 kJ能量 |