已知溴单质的氧化性介于氯和碘之间,利用这一性质解决下面问题。
(1)下列物质或微粒中,在酸性条件下可能氧化Br-的是 (填序号)。
A.I2 B. MnO4- C.MnO2 D.Cl-
(2)把滤纸用淀粉和碘化钾的混合溶液浸泡、晾干后可获得实验常用的淀粉碘化钾试纸。这种试纸润湿后,遇少量氯气可观察到试纸变蓝,用化学方程式解释该现象: 。
(3)下列试剂不能把NaCl和KI两种无色溶液区别开的是 (填序号)。
A.氯水 B.溴水 C.淀粉溶液 D.稀硝酸
(4)100mL溴化 亚铁溶液中通入3.36L氯气(标况),充分反应后测得溶液中氯离子与溴离子的物质的量浓度相等,则原溴化亚铁溶液的物质的量浓度为 。
亚铁溶液中通入3.36L氯气(标况),充分反应后测得溶液中氯离子与溴离子的物质的量浓度相等,则原溴化亚铁溶液的物质的量浓度为 。
某兴趣小组采用如下方法制作氢氧燃料电池。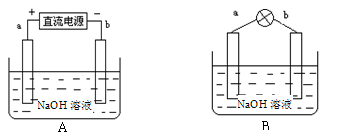
(1)如图A所示:a、b均为多孔石墨棒(多孔石墨棒,可吸附并储存生成的气体),其中a与直流电源正极相连,b与直流电源负极相连,电解质溶液为NaOH溶液,则a电极上发生的电极反应式为_______________,电解后溶液的浓度 ____________(填“增大”、“减小”或“不变”)。
(2)然后如图B所示,移走直流电源,在a、b极间连接一个发光二极管,可以看到二极管发光。此时的电流方向是______________(填“a→b”或“b→a”),b极的电极反应式为________________________。
依据氧化还原反应:Zn(s) + Cu2+(aq) ="=" Zn2+(aq)+ Cu(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是_________ ;电解质溶液Y是_________ ;
(2)铜电极为电池的________极,发生的电极反应为____________ ____ ;X电极上发生的电极反应为______________________。
1gC2H2完全燃烧生成液态水和CO2,放出49.8kJ热量,则2molC2H2完全燃烧放出的热量为 kJ;写出C2H2燃烧的热化学方程式: 。
为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
| 实验目的 |
试剂及方法 |
| 证明地瓜中有淀粉 |
|
| 除去CO2中混有的少量CO |
|
| 检验FeCl2溶液是否变质 |
|
| 除去Na2CO3固体中NaHCO3 |
供选择的化学试剂及实验方法
A.加热 B.滴加碘水
C.加入KSCN溶液 D.通过灼热的CuO
简要回答下列问题。
(1)鉴别胶体与溶液的最简便方法是 。
(2)常温下,浓硝酸可以用铁质容器密封盛放的原因是 。
(3)3月22日是“世界水日”,水是生命之源,没有水就没有生命。请你提出一种有利于保护水资源的措施: 。