下列反应属于取代反应的是
A.CH2=CH2+HBr CH3-CH2 Br CH3-CH2 Br |
B.2CH3CH2OH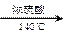 CH3CH2OCH2CH3 + H2O CH3CH2OCH2CH3 + H2O |
C. |
D.CH3CH2OH + HBr CH3CH2Br + H2O CH3CH2Br + H2O |
设阿伏加德罗常数的值为NA,则下列说法正确的是
| A.常温常压下,18.0g NH4+中所含的质子数为10 NA |
| B.111g CaCl2晶体中所含共用电子对的数目为2NA |
| C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
| D.室温下,8 g甲烷含有共价键数为2NA |
下列叙述正确的是
| A.CuSO4·5H2O是一种混合物 |
| B.常温下,pH=1的水溶液中Na+、NO3—、HCO3—、Fe2+可以大量共存 |
| C.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2 |
| D.C(石墨,s)=C(金刚石,s) ;△H>0,所以石墨比金刚石稳定 |
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
|
①2MoS2 + 7O2=== 2MoO3 + 4SO2;②MoO3 + 2NH3·H2O === (NH4)2MoO4 + H2O;
③(NH4)2MoO4 + 2HCl ===== H2MoO4↓ + 2NH4Cl;④ H2MoO4==== MoO3 + H2O;关节炎的病因主要是在关节滑液中形成了尿酸钠(NaUr)晶体,主要反应为: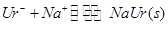 ,第一次关节炎发作往往在冬季,有关该反应的说法正确的是
,第一次关节炎发作往往在冬季,有关该反应的说法正确的是
| A.正反应是吸热反应 | B.正反应是放热反应 |
| C.升高温度平衡向正反应方向移动 | D.以上说法都不正确 |
美国科学家用有机分子和球形笼状分子C60首次制成了“纳米车”(如图),每辆“纳米车”是用一个有机分子和4个球形笼状分子“组装”而成。“纳米车”可以用来运输单个的有机分子,生产复杂的材料和药物,成为“纳米生产”中的有用工具。下列说法正确的是
| A.我们可以直接用肉眼清晰地看到这种“纳米车”的运动 |
| B.“纳米车”的诞生,说明人类操纵分子的技术进入一个新阶段 |
| C.C60是一种新型化合物 |
| D.C60熔点比金刚石熔点高 |