足量的Fe粉与一定量的盐酸反应,为了减慢反应速率,但又不影响产生氢气的总量,应加入下列物质中的
A.NaNO3溶液 B.NaCl固体 C.水 D.CuSO4
有8种物质:①甲烷;②苯;③聚乙烯;④1,3-丁二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧环己烯。既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是
| A.③④⑤⑧ | B.④⑤⑧ | C.④⑤⑦⑧ | D.③④⑤⑦⑧ |
下列实验操作中正确的是
| A.制取溴苯:将铁屑、溴水、苯混合加热 |
| B.实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 |
| C.鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 |
| D.检验卤代烃中的卤原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀的颜色 |
下列各组中两个化学反应,属于同一反应类型的一组是
| A.由苯制硝基苯;由苯制环己烷 |
| B.由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷 |
| C.乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色 |
| D.由苯制溴苯;由乙酸与乙醇反应制乙酸乙酯 |
常温常压下为无色液体,而且密度大于水的是
①苯②硝基苯③溴苯④溴乙烷⑤正己烷⑥四氯化碳⑦CH3Cl⑧丁烯⑨甲苯
| A.②③④⑥ | B.②③④⑥⑨ | C.①②③④⑤⑥⑨ | D.②③⑥⑨ |
某学生用下图1所示装置进行化学反应X+2Y=2Z能量变化情况的研究。当往试管中滴
加试剂Y时,看到U型管中液面甲处降乙处升。关于该反应的下列叙述①该反应为放热反应;
②生成物的总能量比反应物更高;③该反应过程可以看成是“贮存”于X、Y内部的能量转
化为热量而释放出来。其中正确的是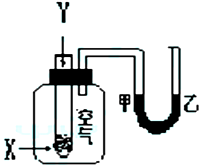
| A.①②③ | B.②③ | C.①② | D.①③ |