下列离子方程式正确的是 ( )
| A.向次氯酸钙溶液中通入少量二氧化硫:Ca2++2ClO—+SO2+H2O=CaSO3↓+2HClO |
B.用Na2CO3溶液作洗涤剂:CO2-3+2H2O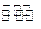 H2CO3+2OH— H2CO3+2OH— |
| C.用碳酸钠溶液吸收少量二氧化硫:2CO2-3+SO2+H2O=2HCO—3+SO2-3 |
D.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO—3+5I—+3H2O=3I2+6OH — — |
浓硝酸和浓硫酸是实验室常用的试剂,下列关于浓硝酸和浓硫酸的叙述正确的是()
| A.分别向其中滴加紫色的石蕊试液,现象都是先变红后褪色 |
| B.常温下都能与铜剧烈反应 |
| C.露置在空气中,容器中酸液的质量都增加 |
| D.露置在空气中,容器中酸液的浓度都降低 |
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图1装置),下列有关说法正确的是()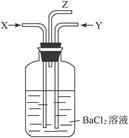
图1
| A.洗气瓶中产生的沉淀是碳酸钡 |
| B.在Z导管出来的气体中无二氧化碳 |
| C.洗气瓶中产生的沉淀是硫酸钡 |
| D.在Z导管口有红棕色气体出现 |
铜和浓硝酸反应产生的气体,用排水法收集到a L气体(标准状况),被还原的硝酸是()
| A.a/22.4 mol |
| B.a/11.2 mol |
| C.3a/22.4 mol |
| D.3amol |
两份质量均为a g的硫,在一定条件下分别跟足量的氢气和氧气完全反应,反应后将生成物混合,析出硫的质量为()
| A.2a g | B.a g | C.1.5a g | D.0.5a g |
酸雨形成的主要原因是()
| A.汽车排放的大量尾气 |
| B.生产硫酸工厂排放的尾气 |
| C.工业上大量含硫燃料的燃烧 |
| D.乱砍滥伐,破坏了生态平衡 |