肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2,且分子中只含有一个苯环,苯环上只有一个取代基。已知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示化学键:单键、双键等)。试回答下列问题。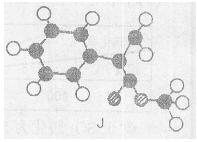
(1)①肉桂酸甲酯(H)的结构简式为 。
②有关肉桂酸甲酯的叙述中,正确的是 (填字母编号)。
| A.能与溴的四氯化碳溶液发生加成反应 |
| B.不能使酸性高锰酸钾溶液褪色 |
| C.在碱性条件下能发生水解反应 |
| D.不可能发生加聚反应 |
(2)现测出A的核磁共振氢谱谱图有6个峰,其面积之比为1:2:2:2:1:2。
用芳香烃A为原料合成H的路线如下: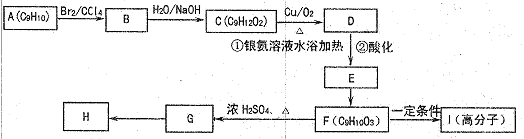
①化合物F中的官能团是 (填名称)。
②B→C的反应类型是 ,F→G的反应类型是 。
③写出下列反应的化学方程式:
F→I: 。G→H: 。
(3)写出符合下列条件的G的所有同分异构体的结构简式: 。
I.分子内含苯环,且苯环上只有一个支链;
II.一定条件下,1mol该物质与足量的银氨溶液充分反应,生成4mol银单质。
某同学用NaCl固体配制200 mL 1 mol/L的NaCl溶液,请回答下列问题。
(1)用托盘天平称取NaCl固体,其质量是______________ g。
(2)实验操作的正确顺序是(填序号)。
①继续加蒸馏水至液面距刻度线1~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切;;
②盖好容量瓶瓶塞,充分摇匀;
③把所得溶液冷却至室温后,小心转入容量瓶中;
④称量固体;
⑤用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶中
⑥ 把称量好的固体放入小烧杯中,加适量蒸馏水溶解。
(3)下列操作对溶液浓度有何影响(填“偏高”、“偏低”或“无影响”):
a.配制溶液时,容量瓶未干燥:
b.配制过程中,没有洗涤烧杯和玻璃棒:
c.定容时,俯视刻度线:
d.从配制好的溶液中取出10 mL :
工业上利用硅的氧化物制取硅单质,主要反应为:SiO2 + 2C  Si + 2CO↑。该反应中,还原剂是(填化学式),被还原的物质是(填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为mol。
Si + 2CO↑。该反应中,还原剂是(填化学式),被还原的物质是(填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为mol。
氯气及其相关产品在生活、生产中应用广泛。
(1)氯气属于有毒气体,在实验室进行相关实验时,除必须进行尾气处理外,还应注意的问题是;若在生活中遇贮氯罐意外泄漏,应(填“顺风”或“逆风”)疏散,消防员喷洒稀NaOH溶液的作用是。(用化学方程式表示)
(2)① 实验室常用NaOH溶液吸收多余的氯气,下列试剂也可用于吸收氯气的是(填字母)。
a. NaCl溶液 b. FeSO4溶液 c. Na2SO3溶液
② 写出①中你选择的吸收试剂与Cl2反应的离子方程式:。
(3)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
①分析“对金属制品有腐蚀作用”的原因。
②需“密闭保存”的原因。
③“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:。
(4)若空气中氯气的含量超过0.1 mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗了0.001 mol/L的KI溶液 100 mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是。
下图为氮及其化合物的类别与化合价对应的关系图。
(1)实验室制取氨气。
① 化学方程式是。
② 可用向下排空气法收集氨气的原因是。
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2  2NO。
2NO。
b. 氨的催化氧化:_________。
② 体现N元素的氧化性:_________。
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。
① NO2溶于水的化学方程式是_________。
② 使试管中NO2完全被水吸收的操作是________。
H2O2是重要的化工原料。
(1)H2O2中O元素的化合价为______。
(2)①向酸性KMnO4溶液中滴加H2O2溶液,溶液褪色,体现了H2O2的还原性,其中氧化过程是:H2O2→______(填化学式)。
②向H2SO4酸化的FeSO4溶液中滴加H2O2溶液,溶液变成黄色,体现了H2O2的氧化性,反应的离子方程式是_________。
(3)H2O2不稳定易分解。实验室需要448 mL O2(标准状况),则理论上最少需要用30%的H2O2溶液(密度为1.10 g/mL)_______mL。(计算结果保留一位小数)