可逆反应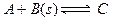 达到平衡后,无论加压或降温。B的转化率都增大,则下列结论正确的是
达到平衡后,无论加压或降温。B的转化率都增大,则下列结论正确的是
A. A为气体,C为固体,正反应为放热反应
B. A为固体,C为气体,正反应为放热反应
C. A为气体,C为固体,正反应为吸热反应
D. A、C均为气体,正反应为吸热反应
下列物质中,不属于烃类的是
| A.乙烷 | B.苯 | C.乙烯 | D.乙醇 |
在周期表中,元素性质呈现周期性变化的本质原因是
| A.中子数逐渐增大 | B.相对原子质量逐渐增大 |
| C.核外电子排布呈现周期性变化 | D.元素化合价呈现周期性变化 |
下列关于化学反应的说法中不正确的是
| A.能量变化是化学反应的基本特征之一 |
| B.能量变化可以体现为热能、光能、电能等 |
| C.化学反应中能量变化的大小与反应物的多少无关 |
| D.化学反应中的能量变化主要原因是化学键的断裂和形成 |
考古学常用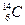 来确定文物的历史年代,
来确定文物的历史年代,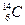 原子核内中子数是
原子核内中子数是
| A.6 | B.8 | C.14 | D.20 |
在元素周期表中,同主族元素原子具有相同的
| A.最外层电子数 | B.核电荷数 | C.电子层数 | D.核外电子数 |