已知:C(s)+CO2(g)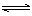 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是
| A.升高温度和减小压强 | B.降低温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和增大压强 |
一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
| A.缩小体积 | B.恒容,充入He | C.恒容,充入O2 | D.恒压,充入N2 |
下列叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.反应是放热反应还是吸热反应,由生成物与反应物的焓值差决定 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
某实验小组以H2O2分解为例,研究浓度、催化剂对反应速率的影响。在常温下按照如下方案完成实验。实验②的反应物应为
| 实验编号 |
反应物 |
催化剂 |
| ① |
10 mL 2% H2O2溶液 |
无 |
| ② |
无 |
|
| ③ |
10 mL 5% H2O2溶液 |
MnO2固体 |
A.5 mL 2% H2O2溶液B.10 mL 5% H2O2溶液
C.10 mL 2% H2O2溶液D.5 mL 10% H2O2溶液
已知在1×105Pa,298K条件下,1mol氢气燃烧生成水蒸气放出242kJ热量,下列热化学方程式正确的是
| A.H2(g)+1/2O2(g)=H2O(g) ΔH=+242kJ·mol-1 |
| B.H2O(g)=H2(g)+1/2O2(g) ΔH=+242kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l)ΔH=-484kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g)ΔH=+484kJ·mol-1 |
工业上常用可逆反应2SO2+O2 2SO3△H<0,制备硫酸,下列对该反应的说法正确的是
2SO3△H<0,制备硫酸,下列对该反应的说法正确的是
| A.增大压强,平衡向逆反应方向移动 |
| B.升高温度,平衡向正反应方向移动 |
| C.当v(SO2):v(O2):v(SO3 )=2:1:2时,反应达到平衡状态 |
| D.当单位时间内生成2 mol SO2的同时生成2 mol SO3,说明该反应达到平衡状态 |