下列说法中错误的是
| A.测定中和热的实验中每次实验需要测定三次温度数据 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.凡经加热而发生的化学反应都是吸热反应 |
| D.反应物总能量和生成物总能量的相对大小决定了反应是放热还是吸热 |
化学与生活息息相关,下列说法正确的是
| A.蔗糖、钡餐(硫酸钡)和水分别属于弱电解质、强电解质和非电解质 |
| B.淀粉、油脂和蛋白质都是高分子化合物 |
| C.用食醋可除去热水壶内壁的水垢 |
| D.光导纤维是将太阳能转化为电能的常用材料 |
一定温度下,在2L恒容密闭容器中发生反应:2N2O5(g) 4NO2(g)+ O2(g)△H﹥0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是
4NO2(g)+ O2(g)△H﹥0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是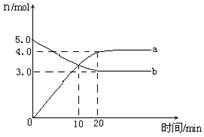
| A.10min时,反应达到平衡 |
| B.达到平衡时N2O5的转化率为60% |
| C.0~20min内平均反应速率v(N2O5)=0.05mol∙L-1∙min-1 |
| D.曲线a表示NO2的物质的量随反应时间的变化 |
对于室温下pH=3的醋酸,下列叙述正确的是
| A.加水稀释后,醋酸的电离程度增大,溶液的导电性增强 |
| B.c(H+)=c(CH3COO-)+c(OH-) |
| C.加入少量醋酸钠固体后,恢复至室温,溶液中c(CH3COO-)∙c(H+)/c(CH3COOH)不变 |
| D.与等体积pH=11的NaOH溶液混合后,pH=7 |
根据下列实验现象得出的结论,正确的是
| 选项 |
实验现象 |
结论 |
| A |
某气体能使润湿的淀粉碘化钾试纸变蓝 |
该气体一定是氯气 |
| B |
向某溶液中加入盐酸酸化的BaCl2,有白色沉淀生成 |
该溶液中一定存在SO42- |
| C |
铁与稀硝酸充分反应后,溶液呈浅绿色 |
稀硝酸与铁反应只能生成Fe2+ |
| D |
SO2通入溴水中,溴水褪色 |
SO2具有还原性 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,11.2 L CH3OH中含有C-H键1.5NA |
| B.9g18 8O2中含有的中子数为5NA |
| C.1 L pH=1的硫酸溶液中含有的H+数为0.2NA |
| D.1 mol Cu与足量S完全反应生成Cu2S,转移电子数为2NA |