(4分)将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应3A(g)+B(g)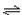 xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min).求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min).求:
(1)此时A的浓度c(A)= mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)= mol。
(2)B的平均反应速率v(B)= mol/(L·min)。 (3)x的值为 。
(8分)已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示。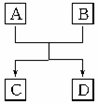
请按要求写出有关反应的化学方程式:
(1)若其中A、D为单质且同主族,B、C为氧化物: (该反应在工业上 有重要用途)。
(2)若A、D为常态下的气体单质且不同主族,B、C为化合物且B为水:。
(3)若A、B、C均为化合物且C为水,单质D常态下为固体:。
(4) 若A、D为固体单质且不同主族,B、C为氧化物:。
(8分)请回答下列各问:
(1)酸雨的pH范围是,在空气质量报告的各项指标中有可吸入颗粒物,还有。
(2)石灰法是目前应用最广泛的工业废气脱硫方法,过程如下:通过煅烧石灰石得到生石灰,以生石灰为脱硫剂在吸收塔中与废气中的SO2反应而将硫固定,写出反应的化学方程式。
(3)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是(填序号)。
① Cu + HNO3(浓)→ Cu(NO3)2
② Cu + HNO3(稀)→ Cu(NO3)2
③ Cu  CuO
CuO Cu(NO3)2
Cu(NO3)2
(4)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是。
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为。
(12分)在一定温度下将 2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)
2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),2分钟末反应达到平衡状态,生
2C(g)+2D(g),2分钟末反应达到平衡状态,生 成了0.8 mol D,请填写下面空白。
成了0.8 mol D,请填写下面空白。
(1) B的平衡浓度为________。
(2) A的转化率为________。
(3) 用D表示的平均反应速率为________。
(4) 如果缩小容器容积(温度不变),达到新平衡时混合气体的密度________、平均相对分子质量________。(两空均选填“增大”、“减小”或“不变”)。
(5)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3 mol,要使平衡时各物质的质量分数与原平衡时相等,则还应加入________mol B物质。
(7分)有A、B、C、D四种无色溶液。它们的溶质分别是Na2CO3、Na2SO4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为:①A+D―→溶液+气体,②B+C―→溶液+沉淀,③B+A―→溶液+沉淀X,④D+B―→溶液Y+沉淀,⑤溶液Y+沉淀X―→溶液+气体。
(1)根据以上记录确定:A________、B________、C________、D________
(填化学式)。
(2)写出①、③、⑤各反应的离子方程式:
①____________________________________________________;
③___ _________________________________________________;
_________________________________________________;
⑤____________________________________________________。
晶体的世界丰富多彩,晶体的结构纷繁复杂。人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、CsCl、CaF2。下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题:
(1)描述晶体结构的单元叫做晶胞,整块晶体可以看作是数量巨大的晶胞而成的。
( 2)某分子晶体的晶胞如上图(B、C球所代表的位置无该分子)所示,则该分子晶体是;该分子晶体中,一个分子周围紧邻个分子。
2)某分子晶体的晶胞如上图(B、C球所代表的位置无该分子)所示,则该分子晶体是;该分子晶体中,一个分子周围紧邻个分子。
(3)若上图是NaCl的晶胞图,则A球代表,B球代表,C球代表。
(4)若上图是金刚石的晶胞图,则碳原子处于位置(选填“A球”、“B球”、“C球”)。
(5)某金属晶体的晶胞如上图(A、C球所代表的位置无该金属原子)所示,则该金属晶体是。