下列关于化学观或化学研究方法的叙述,错误的是
| A.根据元素周期律,由HClO4可类推出氟元素也存在最高价氧化物的水化物HFO4 |
| B.在元素周期表的金属和非金属分界线附近寻找半导体材料 |
| C.控制实验条件可以改变可逆反应的限度和速率 |
| D.在化工生产中应遵循“绿色化学”的思想 |
已知CO(g)十H2O(g) CO2(g)十H2 (g)△H<0 在850 ℃时,其平衡常数K=1,850 ℃时在该容器中同时充入1.0molCO,3.0molH2O,1.0molCO2,5.0molH2,根据所学知识可知
CO2(g)十H2 (g)△H<0 在850 ℃时,其平衡常数K=1,850 ℃时在该容器中同时充入1.0molCO,3.0molH2O,1.0molCO2,5.0molH2,根据所学知识可知
A. 此时反应向正反应方向进行
B. 平衡时CO2的物质的量为0.6mol
C.其他条件不变,向平衡后体系中加入1.0mol CO2,则平衡向左移动,K减小
D. 其他条件不变,向平衡后体系中再加入1.0molCO,3.0molH2O,1.0molCO2,5.0molH2,则平衡向左移动。
已知25℃时,AgCl 的溶度积Ksp=1.8×10-10,则下列说法正确的是
A.向饱和AgCl 水溶液中加入盐酸,Ksp值变大
B.AgNO3溶液与NaCl 溶液混合后的溶液中,一定有c(Ag+)="c(" Cl— )
C.温度一定时,当溶液中c(Ag+)×c( Cl— )=Ksp,此溶液为氯化银的饱和溶液
D 将固体AgCl 加入到较浓的KI 溶液中,部分AgCl会转化为AgI ,所以 AgCl的溶解度小于AgI
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
A.该反应的化学平衡常数表达式是 |
| B.此时B的平衡转化率是40% |
| C.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
| D.增加B,平衡向右移动,B的平衡转化率增大 |
在一密闭容器中,反应aA(g)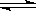 bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡后,A的浓度变为原来的60%,则
bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡后,A的浓度变为原来的60%,则
| A.平衡向正反应方向移动了 | B.平衡向逆反应方向移动了 |
| C.物质B的质量分数增加了 | D.a<b |
常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL0.1000 mol·L-1某一元弱酸HA溶液滴定曲线如图。下列说法正确的是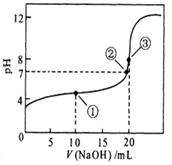
A. 点①所示溶液中:c(A-)+c(OH-) =c(HA) +c(H+)
B. 点②所示溶液中:c(Na+) = c(HA) +c(A-)
C. 点③所示溶液中:c(Na+) > c(A-)> c(OH-) > c(H+)
D. 滴定过程中可能出现:c(HA) > c(A-) > c(H+) > c(OH-)> c(Na+)