扑热息痛是一种优良的解热镇痛剂,其结构式为: ,它不可能具有的化学性质是
,它不可能具有的化学性质是
| A.能与NaOH溶液反应 | B.能与浓溴水发生取代反应 |
| C.能被KMnO4酸性溶液氧化 | D.能发生消去反应 |
从下列实验事实所得出的相应结论不正确的是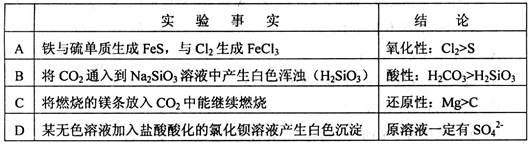
若氧元素只有16O、18O两种核素,下列说法正确的是
| A.16O和18O的物理性质和化学性质完全相同 |
| B.通过化学反应可以实现16O与18O的相互转化 |
C.向2SO2(g)+ O2(g) 2SO3(g)的平衡体系中加入18O2,达到新的平衡后18O只出现在O2与SO3中 2SO3(g)的平衡体系中加入18O2,达到新的平衡后18O只出现在O2与SO3中 |
| D.用惰性电极电解含有H218O的普通水时,阳极可能产生三种相对分子质量不同的氧分子 |
下列关于有机物结构、性质的说法正确的是
| A.石油的分馏和煤的干馏都是化学变化 |
| B.分子式为C3H7C1的有机物有三种同分异构体 |
| C.甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 |
| D.向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
NA代表阿伏加德罗常数的值。下列有关叙述正确的是
| A.含有NA个氮气和乙烯分子的混合气体质量为28g |
| B.标准状况下,11.2L氦气中含有NA个氦原子 |
| C.将NA个NH3分子溶于lL水中得到lmol/L的氨水 |
| D.100mL 0.1mol/LAlCl3溶液含有0.01NA个A13+ |
足量的铝与20mL1.0mol/L的下列物质反应,产生气体物质的量最少的是
| A.氢氧化钠溶液 | B.稀硫酸 |
| C.盐酸 | D.稀硝酸 |