贝诺酯是由阿司匹林、扑热息痛经化学法拼合制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下:
下列叙述错误的是
| A.FeCl3溶液可区别阿司匹林和扑热息痛 |
| B.1mol阿司匹林最多可消耗2mol NaOH |
| C.常温下贝诺酯在水中的溶解度小于扑热息痛 |
| D.C6H7NO 是扑热息痛发生类似酯水解反应的产物 |
下列物质中,能使酸性KMnO4溶液褪色的是
①乙烯②乙烷③乙苯④乙醇⑤乙酸⑥聚乙烯⑦苯
| A.①③⑥ | B.③⑤⑥⑦ | C.①③④ | D.②⑤⑦ |
室温下,向10 mL 0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是 ()
| A.溶液中粒子的数目减小 |
| B.再加入CH3COONa固体能促进醋酸的电离 |
| C.稀释醋酸溶液,溶液中所有离子的浓度均降低 |
D.溶液中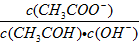 不变 不变 |
某温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是()
4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是()
| A.前2 min,D的平均反应速率为0.2 mol/(L·min) |
| B.此时,B的平衡转化率是40% |
| C.增大该体系的压强,平衡不移动 |
| D.增加B,平衡向右移动,B的平衡转化率增大 |
将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是()
| A.KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B.Cu作负极,发生还原反应 |
| C.电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液 |
| D.工作一段时间后,AgNO3溶液中c(Ag+)减小 |
常温下,下列各组离子在指定溶液中能大量共存的是 ( )
| A.pH=1的溶液中:Fe2+、NO3-、Na+、SO42- |
| B.水电离出的c(H+) =10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+) =0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |