下列排列顺序正确的一组是
| A.半径:Fe(OH)3胶粒>I->K+>Na+ | B.熔沸点:HF<HCl<HBr<HI |
| C.还原性:Fe3+>Cu2+>Fe2+>Zn2+ | D.热稳定性:HF< PH3<H2S<HCl PH3<H2S<HCl |
下列说法正确的是
| A.宏观上的物质对外不显电性,是因为组成它们的微观粒子都是电中性的原子和分子 |
| B.某物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物 |
| C.利用化学方法,我们可以制造出新的分子,但不能制造出新原子 |
| D.由两种元素组成的电解质分子中,显正价的是阳离子,显负价的是阴离子 |
现有阳离子交换膜、阴离子交换膜、石墨电极和如图所示的电解槽。用氯碱工业中的离子交换膜技术原理,可电解Na2SO4溶液生产NaOH溶液和H2SO4溶液。下列说法中正确的是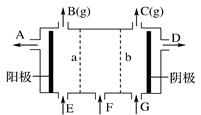
| A.b是阳离子交换膜,允许Na+通过 |
| B.从A口出来的是NaOH溶液 |
| C.阴极反应式为4OH--4e-="=" 2H2O+O2↑ |
| D.Na2SO4溶液从G口加入 |
已知X、 Y、 Z、 W为短周期主族元素,在周期表中的相对位置如图,下列说法正确的是
| A.若 HmXOn为强酸,则 X的氢化物溶于水一定显酸性(m、n均为正整数) |
| B.若四种元素均为金属,则 Z的最高价氧化物对应的水化物一定为强碱 |
| C.若四种元素均为非金属,则 W的最高价氧化物对应的水化物一定为强酸 |
| D.若四种元素中只有一种为金属,则 Z与 Y 两者的最高价氧化物对应的水化物能反应 |
用惰性电极电解CuSO4溶液一段时间,停止后,向所得溶液中加入0.2molCu(OH)2,恰好使溶液恢复至电解前,关于电解过程说法不正确的是
| A.生成的铜的物质的量是0.2mol | B.随着电解进行溶液的pH减小 |
| C.转移电子的物质的量为0.4mol | D.阳极反应是2H2O -4e-=4H+ +O2↑ |
25℃时,将氨水与氯化铵溶液混合得到 c(NH3·H2O)+c(NH4+) =" 0.1" mol·L-1的混合溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如图所示。下列有关离子浓度关系叙述一定正确的是
| A.W点表示溶液中:c(NH4+) +c(H+) = c(OH-) |
| B.pH=10.5溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)<0.1 mol·L-1 |
| C.pH=9.5溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+) |
| D.向W点所表示1L溶液中加入0.05molNaOH固体(忽略溶液体积变化):c(Cl-)>c(Na+)>c(OH-)>c(NH4+)>c(H+) |