从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学反应的是:
| A.对空气进行降温加压 | B.金刚石变成石墨 |
| C.NaCl熔化 | D.碘溶于CCl4中 |
对下列事实的解释正确的是( )
| A.浓硝酸的光照下变黄,说明浓硝酸不稳定,且产物有红棕色气体可溶于浓硝酸。 |
B.向某溶液中加入氯化钡溶液和稀硝酸,有白色沉淀生成,说明该溶液中一定含有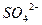 。 。 |
| C.常温下,将铜放入浓硫酸中无明显变化,说明铜在冷、浓硫酸中钝化。 |
| D.氯气使湿润的碘化钾淀粉试纸变蓝,说明氯气与淀粉反应。 |
图19-1装置可用于( )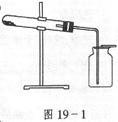
| A.加热无水醋酸钠和碱石灰的混合物,制取甲烷。 |
| B.加热氯酸钾和少量二氧化锰的混合物,制取氧气。 |
| C.加热二氧化锰和浓盐酸的混合物,制取氯气。 |
| D.加热氯化铵和消石灰的混合物,制取氨气。 |
T℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图2所示:
下列描述正确的是
| A.平衡时X、Y的转化率相同 |
| B.达到平衡后,将容器体积压缩为1 L,平衡向正反应方向移动 |
C.T℃时,该反应的化学方程式为:X(g)+Y(g) 2Z(g),平衡常数K=40 2Z(g),平衡常数K=40 |
| D.T℃时,若起始时X为0.71mol,Y为1.00 mol,则平衡时Y的转化率为60% |
下列说法正确的是
A.1 mol  分子中,含17×6.02× 分子中,含17×6.02× 个共用电子对 个共用电子对 |
B.10 mL 18.4 mol· 的浓硫酸与90 mL蒸馏水混合,所得溶液中 的浓硫酸与90 mL蒸馏水混合,所得溶液中 =3.68 mol· =3.68 mol· |
C.25℃时,在pH=4的 溶液与pH=10的 溶液与pH=10的 溶液中,水电离出的 溶液中,水电离出的 前者大于后者 前者大于后者 |
D.在25 mL 0.1 mol·  溶液中,滴入0.1 mol· 溶液中,滴入0.1 mol· 的 的 溶液至混合溶液pH=7时,则滴加 溶液至混合溶液pH=7时,则滴加 溶液的体积大于25 mL 溶液的体积大于25 mL |
下列说法不正确的是
A.向 溶液中滴加氨水,产生白色沉淀,再加入盐酸,沉淀消失 溶液中滴加氨水,产生白色沉淀,再加入盐酸,沉淀消失 |
B.向铜粉中加入稀硫酸,铜粉不溶解;再加入 固体,铜粉溶解 固体,铜粉溶解 |
C.向 溶液中加入 溶液中加入 溶液,产生沉淀,再加入硝酸沉淀全部溶解 溶液,产生沉淀,再加入硝酸沉淀全部溶解 |
D.向 溶液中滴加 溶液中滴加 溶液,产生白色沉淀,再加入 溶液,产生白色沉淀,再加入 溶液,沉淀逐渐变为红褐色 溶液,沉淀逐渐变为红褐色 |