已知某温度下在密闭容器中加入CH3OH,发生如下可逆反应:
2CH3OH(g)==CH3OCH3(g)+H2O(g),反应到某时刻测得各组分的物质的量浓度(mol·L-1)如下,下列有关说法不正确的是( )
| A.10min时v正=v逆 |
| B.5min时该反应速率v(CH3OH)=0.088mol·L-1·min-1 |
| C.该温度下此反应的平衡常数k=400 |
| D.平衡后其它条件不变,升温,c(CH3OH)=0.06mol/L,该反应△H<0 |
根据下列实验装置及现象,可以得到相应结论的是()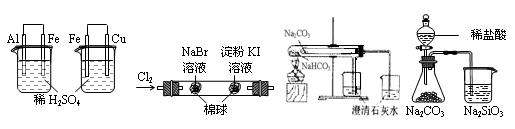
图1图2图3图4
| 实验现象 |
结论 |
|||
|
已知单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为:
a Fe + b NO-3 + c H+ =" d" Fe2+ + f Fe3+ + g NO↑+ h N2O↑+ k H2O化学计量数a~k均为正整数,它们之间的关系错误的是()
| A.c =" 4" g + 10 h | B.c-b ="2" d + 3 f |
| C.2 d + 3 f =" 3" g + 8 h | D.a + c =" d" + f |
设NA为阿伏加德罗常数,下列说法中正确的是()
| A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B.标准状况下,14 g氮气含有的核外电子数为5NA |
| C.1mol金属钠与氧气反应,不论生成氧化钠还是过氧化钠,转移电子数都是NA |
| D.标准状况下,铝跟氢氧化钠溶液反应生成1 molH2时,转移的电子数为NA |
将A与B的混合气体分别置于恒压容器甲和恒容容器乙中,发生如下反应:
|
 2A(g) + 2B(g) 3C(g) ; △H<0.下列说法不正确的是
2A(g) + 2B(g) 3C(g) ; △H<0.下列说法不正确的是 ()
()




一密闭容器中发生反应:2SO2(g)+O2(g)===2SO3(g),
下图表示该反应的速率(v)在某一时间(t)段内
的变化。则下列时间段中,SO3的百分含量最高的
是()
| A.t0→t1 | B.t2→t3 |
C.t3→t4 | D.t5→t6 |