X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
| 元素编号 |
元素性质或原子结构 |
| X |
形成的简单阳离子核外无电子 |
| Y |
元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
| Z |
元素在周期表的族序数等于周期序数的3倍 |
| T |
同周期元素中形成的简单离子半径最小 |
下列说法正确的是( )
A. 原子半径大小顺序:T>Z>Y>X
B. X分别与Y、Z均可形成既含极性键又含非极性键的化合物
C. T的单质与Y的最高价氧化物对应水化物的溶液不反应
D. 由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用
已知:2 CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol根据以上热化学方程式判断,下列说法错误的是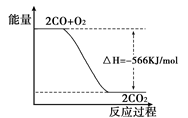
| A.CO2气体分解生成CO气和O2气体的反应是放热反应 |
| B.CO气体与O2气体生成CO2气体的反应是放热反应 |
| C.上图可表示由CO气体生成CO2气体的反应过程和能量关系 |
| D.在相同条件下,2 mol CO气体与1 mol O2气体的能量总和大于2 mol CO2气体的能量 |
用已知物质的量浓度的NaOH溶液测定未知物质的量浓度的盐酸,其操作错误的是
| A.酸式滴定管需用待测盐酸润洗 |
| B.碱式滴定管不用标准碱液润洗 |
| C.滴定过程中不能有液体从锥形瓶溅出 |
| D.滴定结束,读数时要平视读数 |
在固定体积的容器内进行反应2HI(g) 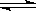 H2(g) + I2(g),达到 平衡状态的标志是
H2(g) + I2(g),达到 平衡状态的标志是
| A.I2(g)的消耗速率等于H2的消耗速率 |
| B.容器中各组分的浓度不随时间变化 |
| C.容器内气体的压强不再变化 |
| D.单位时间内生成n mol H2,同时生成n mol HI |
已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol·L-1、Ka(HF)= 6.8×10-4 mol·L-1、Ka(CH3COOH)= 1.8×10-5 mol·L-1、、Ka(HNO2)= 6.4×10-6mol·L-1。则物质的量浓度都为0.1 mol·L-1的下列溶液中,pH最小的是
| A.NaCN | B.NaF | C.CH3COONa | D.NaNO2 |
下列反应中,属于水解反应且使溶液显酸性的是
A.CH3COOH+OH- CH3COO-+H2O CH3COO-+H2O |
B.HCO3—+ H2O  CO32- + H3O+ CO32- + H3O+ |
C.S2- + H2O HS-+ OH- HS-+ OH- |
D.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |