下列叙述正确的是
| A. | 1.00 中含有6.02×10 23个 分子 |
| B. | 1.00 中,所有 的最外层电子总数为8×6.02×10 23 |
| C. | 欲配置1.00 ,1.00 . 的 溶液,可将58.5 溶于1.00 水中 |
| D. | 电解58.5 熔融的 ,能产生22.4 氯气(标准状况)、23.0 金属钠 |
下列各组气体中均能造成大气污染的是
| A.CO2、O2 | B.N2、NO2 | C.H2S、SO2 | D.Cl2、N2 |
将相同物质的量浓度的某弱酸HX溶液与NaX溶液等体积混合,测得混合溶液中C(Na+)>C(X-),则下列关系错误的是()
| A.C(OH-)<C(H+) | B.C(HX)>C(X-) |
| C.C(X-)+C(HX)=2C(Na+) | D.C(HX)+C(H+)=C(Na+)+C(OH-) |
下列表达式中能精确计算任意浓度[c(NaOH)]的NaOH溶液中氢氧根离子的浓度[c(OH-)]的是(Kw表示水的离子积)()
| A.c(OH-)=c(NaOH) | B.c(OH-)=c(NaOH)+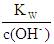 |
| C.c(OH-)=c(NaOH)+KW | D.c(OH-)=c(NaOH)-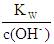 |
在室温下,等体积的酸和碱的溶液混合后,pH一定少于7的是()
| A.pH=3的HNO3跟pH=11的KOH溶液 | B.pH=3的盐酸跟pH=11的氨水 |
| C.pH=3硫酸跟pH=11的氢氧化钠溶液 | D.pH=3的醋酸跟pH=11的氢氧化钠溶液 |
下列说法中不正确的是()
| A.Ksp只与难溶电解质本身的性质和温度有关 |
| B.在一定温度下的AgCl饱和溶液中,C(Ag+)和C(Cl-)的乘积是一个常数 |
| C.在一定温度下,向AgCl饱和溶液中加入盐酸时,Ksp值变大 |
| D.由于Ksp(FeS)>Ksp(CuS),所以FeS沉淀在一定条件下可以转化为CuS沉淀 |