25、101 下:
① ;
②
下列说法正确的是
| A. | ①和②产物的阴阳离子个数比不相等 |
| B. | ①和②生成等物质的量的产物,转移电子数不同 |
| C. | 常温下 与足量 反应生成 ,随温度升高生成 的速率逐渐加快 |
| D. | 25 、101 下, |
分子式为C4H9O2N的有机物,属于氨基酸的同分异构体的有( )
| A.3种 | B.4种 | C.5种 | D.6种 |
下列反应中不属于酯化反应的是( )
A.CH3CH2OH+HO—NO2 CH3CH2ONO2+H2O
CH3CH2ONO2+H2O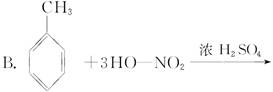
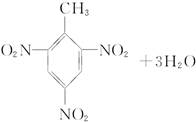
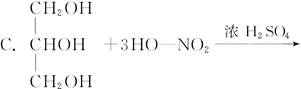
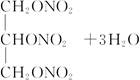
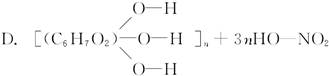
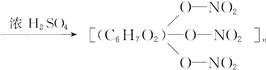 +3nH2O
+3nH2O
下列物质中,不属于酯类的是( )
①酚醛树脂②胶棉③蛋白质④醋酸纤维⑤硬脂酸钠⑥牛油
| A.②④⑥ | B.①③⑤ | C.②④ | D.④⑥ |
为了保护地表的水质,防止河水富营养化,我国对洗衣粉的成分加以限制,其中限制使用的是( )
| A.三聚磷酸钠 |
| B.蛋白酶 |
| C.十二烷基苯磺酸钠 |
| D.硅酸钠 |
下列同组的两物质,不是同分异构体的是( )
| A.乙醇和甲醚 |
| B.苯甲醇和甲基苯酚 |
| C.淀粉和纤维素 |
| D.硝基乙烷和氨基乙酸 |