“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题: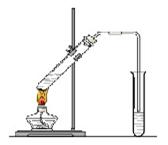
⑴写出制取乙酸乙酯的化学反应方程式:
。
⑵饱和碳酸钠溶液的主要作用是: 。
。
⑶装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑷做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
现有①铁片 ②NaCl溶液③氨水④醋酸⑤酒精⑥盐酸 ⑦H2SO4
⑧KOH固体 ⑨蔗糖 ⑩KAl(SO4)2·12H2O,其中能导电的是,属于电解质的是_______,属于非电解质的是,属于酸的是,属于碱的是。(填序号)
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖。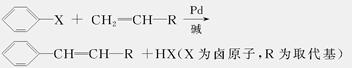

回答下列问题:
(1)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式______。D在一定条件下反应生
成高分子化合物G,G的结构简式是___________________________。
(2)在A→B的反应中,检验A是否反应完全的试剂是_______________________________。
(3)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为_________________________________________________________________________。
有机物A、B、C、D、E、F的转化关系如下: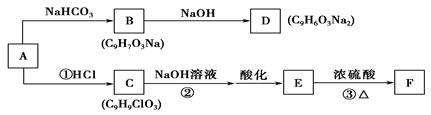
已知:①A是芳香族化合物,其苯环上有2个对位取代基,均不含支链,遇FeCl3溶液能发生显色反应。
②F分子中除了2个苯环外,还含有一个六元环。
请回答下列问题:
(1)A中含有________种官能团,A与足量溴水反应的化学方程式是_______________________。
(2)反应①~③中属于加成反应的有________(填序号)。
(3)C的结构简式为________________,F的结构简式为__________________。
(4)A→B的化学方程式是__________________________________________。
咖啡酸具有止血功效,存在于多种中药中,其结构简式为: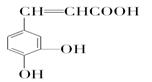
(1)写出咖啡酸中两种含氧官能团的名称:__________________ 、________________。
(2)1mol咖啡酸分别与足量H2、浓溴水和氢氧化钠溶液反应,消耗三种试剂的物质的量依次为:H2__________mol;Br2______________mol;NaOH_____________mol。
(3)蜂胶的分子式为C17H16O4,在一定条件下可水解生成咖啡酸和一种醇A,则醇A的分子式为______________________________。
(4)已知醇A含有苯环,且分子结构中无甲基,写出醇A在一定条件下与乙酸反应的化学方程式:________________________________________________________________。
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_____________,K值大小与温度的关系是:温度升高,K值______________(填“一定增大”、“一定减小”、或“可能增大也可能减小”)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g) 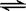 CO2(g)十H2 (g)△H < 0;CO和H2O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)
CO2(g)十H2 (g)△H < 0;CO和H2O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)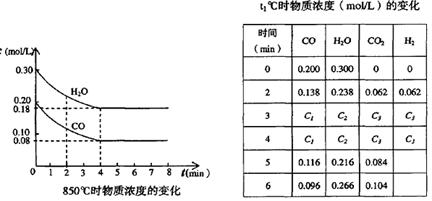
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min—4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min—5min问,平衡向逆方向移动,可能的原因是________(单选), 表中5min—6min之间数值发生变化,可能的原因是__________(单选)。
| A.增加水蒸气 | B.降低温度 |
| C.使用催化剂 | D.增加氢气浓度 |