可逆反应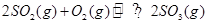 ,从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
,从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
| A.新平衡体系中,SO2和O2物质的量之比仍为2∶1 |
| B.平衡向正反应方向移动了,原因是正反应速率增大了,逆反应速率减小了 |
| C.新平衡体系与旧平衡体系比较,SO3的浓度肯定增大了 |
| D.若所采取的措施是缩小容器的容积,则新平衡SO2和O2转化率之比和旧平衡中SO2和O2的转化率之比都是1∶1 |
在下列溶液中,能大量共存的离子组是( )
A.能使pH试纸显蓝色的溶液中: |
B.常温下 的溶液中: 的溶液中:  |
C.含有大量Al3+的溶液中: |
| D.常温下pH为7的溶液中: K+、Fe3+ 、Cl-、SO42- |
250C时,0.1mol·L-1稀醋酸加水稀释,如图中的纵坐标y可以是( )
| A.溶液的pH | B.醋酸的电离平衡常数 |
| C.溶液的导电能力 | D.醋酸的电离程度 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是()
| A.氢氧燃料电池的负极反应式:O2 + 2H2O+ 4e- = 4OH - |
| B.铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S)-2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq) |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- = Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - = Fe2+ |
关于下列过程熵变的判断不正确的是( )
A.溶解少量食盐于水中, |
B.纯碳和氧气反应生成 |
C.H2O(g)变成液态水, |
D.CaCO3(s)加热分解为CaO和CO2(g), |
下列有关实验的叙述中,合理的是
| A.用pH试纸测得氯水的pH为2 |
| B.电解氯化镁溶液在阴极析出金属镁。 |
| C.向Na2CO3与NaOH的混合溶液中只需加入酚酞试液,即可确认NaOH的存在 |
| D.实验室配制氯化亚铁溶液时,可先将氯化亚铁溶解在盐酸中,再加入蒸馏水稀释,最后加入少量铁屑 |