乙烯是重要化工原料,其产量是一个国家石油化工水平的标志。请回答:
(1) 乙烯通入溴的四氯化碳溶液中,观察到的 现象是 ;其反应方程式为 ;乙烯在一定条件下
现象是 ;其反应方程式为 ;乙烯在一定条件下
发生加聚反应的化学方程式为 。
(2) (6分)此外,乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
[工艺一]: 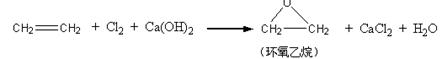
[工艺二]:
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应, 上述工艺一的原子利用率 100%(填“>”、“=”、“<”。下同);工艺二的原子利用率为 100
上述工艺一的原子利用率 100%(填“>”、“=”、“<”。下同);工艺二的原子利用率为 100 %。因此,在实际生产中,应采用工艺 更环保、更经济。
%。因此,在实际生产中,应采用工艺 更环保、更经济。
人在虚脱后需迅速补充葡萄糖。下图是医院给病人输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写:
(1)该溶液的密度为________ g/mL;
(2)该溶液的物质的量浓度为________ mol/L(精确到小数点后面两
位)。
下图是初中化学中常见物质间的转化关系。其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体且1 mol E中含有 10 mol电子。乙和丁为黑色固体,将它们混和加热后发现固体由黑色变为红色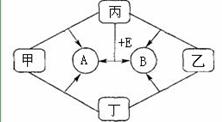
(1)写出化学式:甲_________ ;乙________;丙_______;
(2)丁的摩尔质量为_________ 。
(3)写出丙和E反应生成A和B的化学方程式: ____________________________
(4)有学生将乙和丁混和加热后收集到标准状况下气体8.96 L ,测得该气体对氢气的相对密度为16,若将气体通入足量的澄清石灰水中,得到白色沉淀物g
(9分)某实验需要200mL、0.1mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的g固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用________(填仪器名称)搅拌;②把①所得溶液冷却到室温后,小心转入________(填仪器名称);③继续加蒸馏水至液面至刻度线1~2cm处,改用________(填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切;④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是________(填序号)。
(2)若没有操作④,则所配溶液的浓度会________(填“偏高”或“偏低”)。
(3)若所配溶液的密度为1.06g/mL,则该溶液的质量分数为________。
(4)若取出20mL配好的Na2CO3溶液,加蒸馏水稀释成c(Na+)=0.01mol/L的溶液,则稀释后溶液的体积为________mL。
(5)在配制100mL、0.1mol/L的Na2CO3溶液时,下列操作中的________会导致结果偏低(请用序号填写)。
①用托盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④定容时仰视刻度线
⑤干净的容量瓶未经干燥就用于配制溶液
(5分)对于混合物的分离或提纯,常采用的方法有:①过滤,②蒸发,③蒸馏,④萃取,⑤加热分解等。下列各组混合物的分离或提纯应采用什么方法?(要求:填序号)
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用________的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
(2)提取碘水中的碘,用________方法。
(3)除去食盐溶液中的水,可采用________的方法。
(4)淡化食盐水,可采用______的方法。 (5)除去氧化钙中的碳酸钙可用______的方法。
(7分)(1)1.5molH2SO4的质量是______,其中含有____mol H。
(2)3.6gH2O的物质的量是,含有H2O个。
(3)9.03×1023个氨分子含________摩尔氨分子。
(4)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为。
(5)从1L 1mol/LNaOH溶液中取出100mL,则这100mLNaOH溶液中含NaOH的质量g。