物质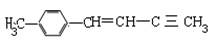 分子中最多有几个碳原子在同一平面上
分子中最多有几个碳原子在同一平面上
| A.8 | B.9 | C.10 | D.11 |
某烃经催化加氢后,不能得到2-甲基丁烷,该烃是
| A.2-甲基-1-丁烯 | B.2-甲基-2-丁烯 | C.3-甲基-1-丁炔 | D.3,3-二甲基-1-丁炔 |
下列事实不能用有机物分子内基团间的相互作用解释的是
| A.苯酚能跟NaOH溶液反应而乙醇不能 |
| B.乙烯能发生加成反应而乙烷不能 |
| C.甲苯能使KMnO4酸性溶液褪色而乙烷不能 |
| D.苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 |
等质量的单质A和化合物B分别和足量水反应产生C、D两种气体单质。一定条件下,产生的C和D两种气体单质恰好可完全反应,则下列判断中正确的是
A. A和B的摩尔质量相同
B. 组成A、B的元素均为短周期元素
C. 等质量的A和B所含的质子数相同
D. 等物质的量的A和B与足量水反应产生的气体的体积比为(同温同压下)为2:1
某学生设计了如下图中的方法对A盐进行鉴定: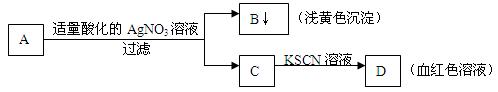
由此分析,下列结论中,正确的是
| A.A中一定有Fe3+ | B.C中一定有Fe3+ |
| C.B为AgI沉淀 | D.A一定为FeBr2溶液 |