有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸中,A极为负极;②C、D用导线相连后,同时浸入稀硫酸中,电流由D→导线→C;
③B、C相连后,同时浸入稀硫酸中,C极产生大量气泡;④B、D相连后,同时浸入稀硫酸中,D极产生大量气泡。据此,判断四种金属的活动性顺序是
A.A>B>C>D B.A>C>D>B
C.C>A>B>D D.B>D>C>A
下列关于化工生产原理的叙述错误的是( )
①可以用电解熔融的氯化钠的方法来制取金属钠
②可以用钠加入氯化镁饱和溶液中制取镁
③可电解冶炼铝,原料是氯化铝
④炼铁高炉中所发生的反应都是放热的,故无需加热
| A.①② | B.②③ |
| C.①②③ | D.②③④ |
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是( )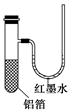
| A.实验中发生的反应都是氧化还原反应 |
| B.铝是一种较活泼的金属 |
| C.铝与氧气反应放出大量的热量 |
| D.铝片上生成的白毛是氧化铝和氧化汞的混合物 |
海水是镁的主要来源之一。从海水中提取镁可按如下步骤进行:
①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥产物;④电解得到产物。
下列关于提取镁的说法中,不正确的是( )
| A.此法的优点之一是原料取自大海 |
| B.进行①②③步骤的目的是富集MgCl2 |
| C.可用电解熔融氧化镁的方法制取镁 |
| D.电解冶炼镁要消耗大量电能 |
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
| A.②④⑤③① | B.③②④①⑤ |
| C.③④②⑤① | D.②④③⑤① |
在氧气中灼烧0.8g由硫、铁元素组成的化合物,使其中的硫经过一系列变化最终全部转化为硫酸,用20 mL 1 mol·L-1的烧碱溶液恰好能完全中和这些硫酸,则原混合物中硫的质量分数约为()。
| A.40% | B.46% | C.53.3% | D.80 % |