下列每组中各有三对物质,它们都能用分液漏斗分离的是
| A.乙酸乙酯和水,酒精和水,植物油和水 | B.四氯化碳和水,溴苯和水,硝基苯和水 |
| C.甘油和水,乙酸和水,乙酸和乙醇 | D.酒精和水,苯和水,己烷和水 |
碘是人体必需的微量元素。碘的一种核素是 ,关于
,关于 的说法中正确的是
的说法中正确的是
| A.核电荷数为53 |
| B.中子数为127 |
| C.质子数为74 |
| D.核外电子数为127 |
有关新制氢氧化铁胶体的说法正确的是
| A.不能透过滤纸 | B.其分散质粒子直径小于1 nm |
| C.能产生丁达尔效应 | D.不能与硫酸反应 |
下列各项中表达正确的是
A. H、D、T表示同一种核素
B.次氯酸电子式
C. F原子结构示意图:
D.CH4分子的球棍模型: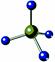
氢气能在某黄绿色的单质气体中安静的燃烧,该单质所含元素位于元素周期表的
| A.第二周期ⅤA族 | B.第三周期ⅣA族 | C.第三周期ⅥA族 | D.第三周期ⅦA族 |
下列四组物质中,互为同位素是
| A.O2和O3 | B.H216O和H218O | C.12C和14C | D.正丁烷和异丁烷 |