氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1molH2中的化学键消耗的能量为Q1kJ,破坏1molCl2中的化学键消耗的能量为Q2kJ,形成1molHCl中的化学键释放的能量为Q3kJ。下列关系式中,正确的是
| A.Q1+Q2>Q3 | B.Q1+Q2>2Q3 | C.Q1+Q2<Q3 | D.Q1+Q2<2Q3 |
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列说法正确的是
| A.白色沉淀是CuI2,棕色溶液含有I2 |
| B.滴加KI溶液时,转移1mol电子时生成1mol白色沉淀 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:I2>Cu2+>SO2 |
在恒温恒容条件下,向容积为2L的密闭容器中充人2. 0 mol SO2和2. 0 mol O2。巳知: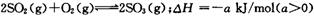 ,经2 min达到平衡状态,反应放热0. 25a kJ。下列判断正确的是
,经2 min达到平衡状态,反应放热0. 25a kJ。下列判断正确的是
A.在1 min时: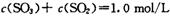 |
B.2 min内: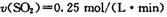 |
| C.若再充入2mol SO3,达平衡时SO3 %(质量分数)减小 |
| D.反应条件相同,若起始时向反应容器中充入2mol SO3,平衡时反应吸热0. 75a kJ |
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是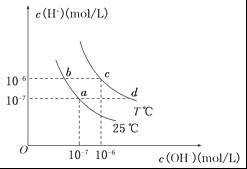
| A.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO |
| B.b点对应的溶液中大量存在:NH、Ba2+、OH-、I- |
| C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO |
| D.d点对应的溶液中大量存在:Na+、K+、SO、Cl— |
在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是
A.分散质微粒的大小与分散系种类的关系: |
B.常温下溶液的pH其酸碱性的关系: |
C.硫的化合物中化合价与其氧化性、还原性的关系: |
D.Fe在Cl2中燃烧的产物与 的关系: 的关系: |
下列有关溶液中微粒的物质的量浓度关系正确的是
| A.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
| B.物质的量浓度相等的①NH4HCO3溶液、②NH4Cl溶液、③NH4HSO4溶液中,c(NH4+)的大小关系:①>②>③ |
| C.0.1 mol·L-1 CH3COONa 溶液与0.05 mol·L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
| D.0.1mol·L-1(NH4)2Fe(SO4)2溶液中: c(NH4+)+ c(NH3·H2O) + c(Fe2+)="0.3" mol·L-1 |