2006年11月23日中科院网报道,纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和作为药物载体用于疾病的治疗。其制备过程如下: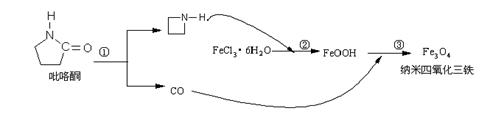
下列叙述不合理的是:
| A.Fe3O4可以表示为FeO·Fe2O3,属于混合物 |
B.在反应②中FeCl3•6H2O被环丙胺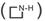 还原为FeOOH 还原为FeOOH |
| C.纳米四氧化三铁分散在适当分散剂中,形成的分散系可能有丁达尔现象 |
| D.反应③的化学方程式是:6FeOOH +CO = 2Fe3O4 +3H2O + CO2 |
用惰性电极实现电解,下列说法正确的是()
| A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |
| B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 |
| C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2 |
| D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1 |
关于电解NaCl水溶液,下列叙述正确的是()
| A.电解时在阳极得到氯气,在阴极得到金属钠 |
| B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 |
| C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
| D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |
下列关于铜电极的叙述中正确的是()
| A.铜锌原电池中铜是负极 |
| B.用电解法精炼粗铜时粗铜作阳极 |
| C.在铁上电镀铜时用铜作阴极 |
| D.电解稀硫酸时用铜作阳极,阳极产物为氧气 |
如下图所示是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是()
| A.a为负极,b为正极 | B.a为阳极,b为阴极 |
| C.电解过程中,d电极质量增加 | D.电解过程中,氯离子浓度不变 |
电工操作中规定不能把铜线和铝线拧在一起连接线路,这是因为()
| A.延伸性相差大,易折断 | B.铝线上的氧化膜电阻大 |
| C.铝线很快被腐蚀 | D.电阻率不同拧在一起要发热 |