下列说法正确的是 
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
| A.①③⑤ | B.②④⑥ | C.②③④ | D.①③⑥ |
某烯烃与氢气加成后得到2,2-二甲基丁烷,该烃的名称是()
| A.3,3,3-三甲基-1-丁炔 | B.2,2-二甲基-2-丁烯 |
| C.2,2-二甲基-1-丁烯 | D.3,3-二甲基-1-丁烯 |
可逆反应aX(g)+b Y(g)  cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(u)一时间(t)图象如下图。则下列说法中正确的是()
cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(u)一时间(t)图象如下图。则下列说法中正确的是()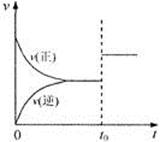
| A.若a+b=c,则t0时只能是增大了容器的压强 |
| B.若a+b=c,则t0时只能是加入了催化剂 |
| C.若a+b≠c,则t0时只能是增大了容器的压强 |
| D.若a+b≠c,则t0时只能是加入了催化剂 |
可以证明可逆反应N2 + 3H2 2NH3已达到平衡状态的是()
2NH3已达到平衡状态的是()
①一个N≡N断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均式量不再改变
④保持其它条件不变时,体系压强不再改变
⑤NH3%、N2%、H2%都不再改变
⑥恒温恒容时,密度保持不变
⑦正反应速率v(H2)=0.6mol/L·min,逆反应速率v(NH3)=0.4mol/L·min
| A.全部 | B.只有①③④⑤ | C.②③④⑤⑦ | D.只有①③⑤⑥⑦ |
恒温恒容下,往一真空密闭容器中通入一定量的气体A,发生如下反应:
3A(g) 2B(g)+xC(g)。达平衡后,测得容器内的压强增大了p%,A的平衡转化率为a%,则下列推断中正确的是()
2B(g)+xC(g)。达平衡后,测得容器内的压强增大了p%,A的平衡转化率为a%,则下列推断中正确的是()
| A.若x=2,则p>0.5a | B.若x=3,则p>0.7a |
| C.若x=4,则p= a | D.若x= 5,则p≥a |
下列有关化学反应速率的说法中,正确的是()
| A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C.二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |